Ген — Википедия
В другом языковом разделе есть более полная статья Gene (англ.).Ген (др.-греч. γένος — род) — в классической генетике — наследственный фактор, который несёт информацию об определённом признаке или функции организма, и который является структурной и функциональной единицей наследственности. В таком качестве термин «ген» был введён в 1909 году датским ботаником, физиологом растений и генетиком Вильгельмом Йоханнсеном[1].
После открытия нуклеиновых кислот в качестве носителя наследственной информации определение гена изменилось, и ген стали определять как участок ДНК (у некоторых вирусов — участок РНК), задающий последовательность полипептида либо функциональной РНК[2].
По мере накопления сведений о строении и работе генов определение понятия «ген» продолжало изменяться, однако в настоящее время не существует универсального определения гена, которое удовлетворило бы всех исследователей[3][4][4]
Совокупность генов организма составляют генотип. Генотип наряду с факторами окружающей среды и развитием определяют, каким будет фенотип. Передача генов потомству является основой наследования фенотипических признаков. Большинство биологических признаков являются полигенными, то есть находятся под влиянием многих генов. Гены могут изменяться в результате мутаций, изменяющих последовательность ДНК. Вследствие мутаций в популяции гены существуют в различных вариантах, называемых аллелями. Разные аллели гена могут кодировать различающиеся версии белка, что может проявляться фенотипически. Гены наряду с участками ДНК, не содержащими генов, входят в состав генома, представляющего собой весь наследственный материал организма.
Обнаружение генов как дискретных носителей наследственности[править | править код]
Грегор МендельЭкспериментальные доказательства наличия дискретных факторов наследственности впервые были представлены в 1865 году Грегором Менделем в докладе на заседании Общества естествоиспытателей в Брно. В 1866 году доклад был опубликован в печатном виде
Следует отметить, что до работы Менделя доминирующей концепцией в объяснении закономерностей наследования была концепция, которая предполагала, что признаки родителей у потомков смешиваются аналогично смешиванию жидкостей. Этой концепции следует теория пангенезиса, разработанная Чарльзом Дарвином в 1868 году, два года спустя после публикации результатов Менделя
Статья Менделя осталась практически незамеченной после её публикации в 1866 году, но она получила второе «рождение» в конце 19-го века, благодаря Хуго де Фризу, Карлу Корренсу и Эриху фон Чермаку, которые пришли к аналогичным выводам в своих собственных исследованиях
В 1909 году Вильгельм Йоханнсен ввел термин «ген»[1], а Уильям Бейтсон — термин «генетика»[11], в то время как Эдуард Страсбургер все ещё использовал термин «панген» для обозначения основной физической и функциональной единицы наследственности[12]
Открытие ДНК в качестве носителя генетической информации[править | править код]
Эксперименты, проведённые в 40-е годы американскими бактериологами из Рокфеллеровского института под руководством О. Эвери, показали, что молекулярным хранилищем генетической информации является ДНК. В работах по генетической трансформации пневмококков было показано, что передача признаков от одних бактерий к другим происходит при помощи только одного вещества — ДНК. Ни белок, ни другие химические компоненты клетки этим свойством не обладали [13][14][15]. В 1953 году при помощи рентгеновской кристаллографии Розалинд Франклин и Морис Уилкинс получили высококачественные снимки структуры ДНК. Эти снимки помогли Джеймсу Д. Уотсону и Фрэнсису Крику создать модель молекулы двуцепочечной спирали ДНК и сформулировать гипотезу механизма генетической репликации
В начале 1950-х годов преобладало мнение, что гены в хромосоме действуют как отдельные объекты, неразделимые путем рекомбинации и расположенные как бусы на веревочке. Эксперименты Сеймура Бензера с использованием мутантов, дефектных бактериофагов в области rII T4[en] (1955—1959), показали, что отдельные гены имеют простую линейную структуру и, вероятно, эквивалентны линейному сечению ДНК[18][19].
В совокупности этот объём исследований установил центральную догму молекулярной биологии, которая утверждает, что белки транслируются с РНК, которая транскрибируется с ДНК. Эта догма с тех пор, как было показано, имеет исключения, такие как обратная транскрипция в ретровирусах. Современное исследование генетики на уровне ДНК известно как молекулярная генетика.
В 1972 году Уолтер Файерс и его команда первыми определили последовательность гена: последовательность белка оболочки Bacteriophage MS2 (англ.)русск.[20]. Последующее развитие секвенирования ДНК с Методом Сэнгера в 1977 году Фредериком Сангером улучшило эффективность секвенирования и превратило его в рутинный лабораторный инструмент[21]. Автоматизированная версия метода Сангера использовалась на ранних этапах проекта «Геном человека»[22].
Современный синтез и его преемники[править | править код]
Эволюционные биологи впоследствии модифицировали эту концепцию, такую как геноцентричный взгляд[en] Джорджа Уильямса на эволюцию. Он предложил эволюционную концепцию гена как единицы естественного отбора с определением: «то, что разделяет и рекомбинирует с заметной частотой»[24]:24. С этой точки зрения, молекулярный ген транскрибируется как единое целое, а эволюционный ген наследуется как единое целое. Связанные идеи, подчеркивающие центральную роль генов в эволюции, были популяризированы Ричардом Докинзом
ДНК[править | править код]
Генетическая информация у подавляющего большинства организмов закодирована в длинных молекулах ДНК. ДНК состоит из двух спирально закрученных полимерных цепей, мономерами которых служат четыре нуклеотида: аденозин, цитидин, гуанозин и тимидин. Нуклеотиды в ДНК состоят из пятиуглеродного сахара (2-дезоксирибозы), фосфатной группы и одного из четырёх азотистых оснований: аденина, цитозина, гуанина и тимина[27]:2.1. Азотистое основание связано гликозидной связью с пятиуглеродным (пентозного) сахаром в 1′-положении. Остовом цепей ДНК служит чередующаяся последовательность пентозных сахаров и фосфатов, фосфатные группы присоединяются к сахару в 5′- и 3′-положениях. Здесь следует отметить, что номера позиций пентозного кольца отмечены штрихом для того, чтобы различать нумерацию колец в сахаре и азотистом основании
Из-за химического состава пентозных остатков цепи ДНК имеют направленность. Один конец полимера ДНК содержит открытую гидроксильную группу на дезоксирибозе в 3′-положении; этот конец называется 3′-конец. Другой конец содержит открытую фосфатную группу, это 5′-конец. Две цепи (нити) двойной спирали ДНК ориентированы в противоположных направлениях. Синтез ДНК, в том числе при репликации ДНК, происходит в направлении 5 ‘→ 3’, потому что новые нуклеотиды добавляются посредством реакции дегидратации, которая использует открытый 3’-гидроксил в качестве нуклеофила
Экспрессия генов, закодированных в ДНК, начинается с транскрипции нуклеотидной последовательности ДНК в последовательность нуклеотидов другого типа нуклеиновых кислот — РНК. РНК очень похожа на ДНК, но её мономеры содержат рибозу, а не дезоксирибозу. Кроме того, вместо тимина в РНК используется урацил. Молекулы РНК являются одноцепочечными и менее стабильны, чем ДНК. Гены белков содержат кодирующую последовательность, состоящую из серии тринуклеотидных блоков — триплетов, которые соответствуют аминокислотам. Правило, по которому определяется, какому триплету соответствует какая аминокислота, называется генетическим кодом. Считывание генетического кода происходит в рибосоме во время трансляции РНК в белок. Генетический код почти одинаков для всех известных организмов
Хромосома[править | править код]
Изображение нормального женского кариотипа, полученного при помощи флуоресцентной микроскопии и метода FISH. ДНК окрашена в красный цвет, а участки хромосом, обогащённые по числу локализованных в них генов, окрашены в зелёный цвет. Самые большие хромосомы примерно в 10 раз больше самых маленьких[30].Наследственный материал организма, или геном, хранится в одной или нескольких хромосомах, число которых специфично для вида. Хромосома состоит из одной очень длинной молекулы ДНК, которая может содержать тысячи генов[27]:4.2. Область хромосомы, где находится ген, называется локусом. Каждый локус содержит определённый аллель гена. Представители популяции могут отличаться по аллелям гена, находящимся в одинаковых локусах хромосом.
Большинство эукариотических генов хранятся в нескольких линейных хромосомах. Хромосомы упакованы в ядре в комплексе с белками хроматина. Наиболее многочисленными белками хроматина являются гистоны, которые формируют белковую глобулу, называемую нуклеосомой. ДНК обвивается вокруг нуклеосом, что представляет собой первый уровень упаковки ДНК в хромосоме[27]:4.2. Распределение нуклеосом вдоль ДНК, а также химические модификации самих гистонов регулируют доступность ДНК для регуляторных факторов, участвующих в транскрипции, репликации, репарации. Помимо генов эукариотические хромосомы содержат также служебные последовательности, обеспечивающие стабильность и воспроизведение хромосом, а также их распределение между дочерними клетками в митозе. Это теломеры, сайты инициации репликации и центромера, соответственно[27]:4.2.
Трудно точно определить, в какую часть последовательности ДНК входит ген[5].
В настоящее время в молекулярной биологии установлено, что гены — это участки ДНК, несущие какую-либо целостную информацию — о строении одной молекулы белка или одной молекулы РНК. Эти и другие функциональные молекулы определяют развитие, рост и функционирование организма.
В то же время каждый ген характеризуется рядом специфических регуляторных последовательностей ДНК (англ.)русск., таких как промоторы, которые принимают непосредственное участие в регулировании проявления гена. Регуляторные последовательности могут находиться как в непосредственной близости от открытой рамки считывания, кодирующей белок, или начала последовательности РНК, как в случае с промоторами (так называемые cis-регуляторные элементы, англ. cis-regulatory elements), так и на расстоянии многих миллионов пар оснований (нуклеотидов), как в случае с энхансерами, инсуляторами и супрессорами (иногда классифицируемые как trans-регуляторные элементы, англ. trans-regulatory elements). Таким образом, понятие гена не ограничено только кодирующим участком ДНК, а представляет собой более широкую концепцию, включающую в себя и регуляторные последовательности.
Изначально термин «ген» появился как теоретическая единица передачи дискретной наследственной информации. История биологии помнит споры о том, какие молекулы могут являться носителями наследственной информации. Большинство исследователей считали, что такими носителями могут быть только белки, так как их строение (20 аминокислот) позволяет создать больше вариантов, чем строение ДНК, которое составлено всего из четырёх видов нуклеотидов. Позже было экспериментально доказано, что именно ДНК включает в себя наследственную информацию, что было выражено в виде центральной догмы молекулярной биологии.
Гены могут подвергаться мутациям — случайным или целенаправленным изменениям последовательности нуклеотидов в цепи ДНК. Мутации могут приводить к изменению последовательности, а следовательно изменению биологических характеристик белка или РНК, которые, в свою очередь, могут иметь результатом общее или локальное изменённое или анормальное функционирование организма. Такие мутации в ряде случаев являются патогенными, так как их результатом является заболевание, или летальными на эмбриональном уровне. Однако далеко не все изменения последовательности нуклеотидов приводят к изменению структуры белка (благодаря эффекту вырожденности генетического кода) или к существенному изменению последовательности и не являются патогенными. В частности, геном человека характеризуется однонуклеотидными полиморфизмами и вариациями числа копий (англ. copy number variations), такими как делеции и дупликации, которые составляют около 1 % всей нуклеотидной последовательности человека[31]. Однонуклеотидные полиморфизмы, в частности, определяют различные аллели одного гена.
Мономеры, составляющие каждую из цепей ДНК, представляют собой сложные органические соединения, включающие в себя азотистые основания: аденин (А), тимин (Т), цитозин (Ц), гуанин (Г), пятиатомный сахар (пентозу) — дезоксирибозу, по имени которой и получила название сама ДНК, — а также остаток фосфорной кислоты. Эти соединения носят название нуклеотидов.
Мутация[править | править код]
Репликация ДНК по большей части чрезвычайно точна, однако ошибки (мутации) случаются[27]:7.6. Частота ошибок в эукариотических клетках может составлять всего 10−8 в нуклеотиде на репликацию[32][33], тогда как для некоторых РНК-вирусов она может достигать 10−3[34]. Это означает, что в каждое поколение, каждый человек в геноме накапливает 1-2 новые мутации[34]. Небольшие мутации могут быть вызваны репликацией ДНК и последствиями повреждения ДНК и включают точечные мутации, в которых изменяется одно основание, и мутации со сдвигом рамки, в которых одно основание вставляется или удаляется. Любая из этих мутаций может изменить ген по миссенс (изменить код для кодирования другой аминокислоты) или по нонсенс (преждевременный стоп-кодон)[35]. Большие мутации могут быть вызваны ошибками в рекомбинации, чтобы вызвать хромосомные аномалии, включая дублирование, делецию, перегруппировку или инверсию больших участков хромосомы. Кроме того, механизмы восстановления ДНК могут вносить мутационные ошибки при восстановлении физического повреждения молекулы. Восстановление, даже с мутацией, является более важным для выживания, чем восстановление точной копии, например, при восстановлении двухцепочечных разрывов[27]:5.4.
Когда в популяции вида присутствует несколько различных аллелей гена, это называется полиморфизм. Большинство различных аллелей функционально эквивалентны, однако некоторые аллели могут вызывать различные фенотипические признаки. Самый распространенный аллель гена называется диким типом, а редкие аллели — мутантами. Генетические различия в относительных частотах различных аллелей в популяции обусловлены как естественным отбором, так и генетическим дрейфом[36]. Аллель дикого типа не обязательно является предком менее распространенных аллелей и не обязательно более приспособлена.
Количество генов[править | править код]
Размер генома и количество генов, которые он содержит, значительно варьируют у таксономических групп. Наименьший геном встречаются у вирусов[37], и вироидов (которые действуют как один некодирующий ген РНК)[38]. И наоборот, растения могут иметь очень большие геномы[39], в рисе содержатся более 46 000 генов, кодирующих белок[40]. Общее количество кодирующих белок генов (протеома Земли) оценивается в 5 миллионов последовательностей[41].
Генная инженерия — это методы модификации генетического материала для изменения свойств живого организма. С 1970-х годов было разработано множество методов, специально предназначенных для добавления, удаления и редактирования генов в вирусах, бактериях, растениях, грибах и животных, включая человека[42]. Недавно разработанные методы геномной инженерии используют инженерные нуклеазные ферменты для создания целевой репарации ДНК в хромосоме, чтобы либо разрушить, либо отредактировать ген в процессе репарации искусственно внесённого разрыва ДНК[43][44][45][46]. Связанный термин синтетическая биология иногда используется для обозначения обширной дисциплины генной инженерии организма[47].
Генная инженерия в настоящее время является рутинным инструментом при работе с модельными организмами. Например, гены легко добавляются к бактериям[48], а линии «Knockout mouse (англ.)русск.» мышей с нарушенной функцией определённого гена используются для исследования функции этого гена[49][50]. Многие организмы были генетически модифицированы для применения в сельском хозяйстве, промышленной биотехнологии и медицине.
У многоклеточных организмов обычно модифицируется эмбрион, который вырастает во взрослый генетически модифицированный организм[51]. Однако геномы клеток взрослого организма можно редактировать с использованием методов генной терапии для лечения генетических заболеваний.
- дискретность — несмешиваемость генов;
- стабильность — способность сохранять структуру;
- лабильность — способность многократно мутировать;
- множественный аллелизм — многие гены существуют в популяции во множестве молекулярных форм;
- аллельность — в генотипе диплоидных организмов только две формы гена;
- специфичность — каждый ген кодирует свой признак;
- плейотропия — множественный эффект гена;
- экспрессивность — степень выраженности гена в признаке;
- пенетрантность — частота проявления гена в фенотипе;
- амплификация — увеличение количества копий гена[источник не указан 1907 дней].
- Структурные гены — гены, кодирующие информацию о первичной структуре белка. Расположение нуклеотидных триплетов в структурных генах коллинеарно последовательности аминокислот в полипептидной цепи, кодируемой данным геном (См. также статью гены домашнего хозяйства).
- Функциональные гены — гены, которые контролируют и направляют деятельность структурных генов[52].
- ↑ 1 2 Johannsen, W. (1905). Arvelighedslærens elementer («The Elements of Heredity». Copenhagen). Rewritten, enlarged and translated into German as Elemente der exakten Erblichkeitslehre (Jena: Gustav Fischer, 1909; Scanned full text.
- ↑ Тарантул В. З. Толковый словарь по молекулярной и клеточной биотехнологиию Русско-английский. — М: Языки славянской литературы, 2015. — Т. 1. — С. 370—371. — 984 с. — ISBN 978-5-94457-249-3.
- ↑ Pearson H. Genetics: what is a gene? (англ.) // Nature. — 2006. — May (vol. 441, no. 7092). — P. 398—401. — DOI:10.1038/441398a. — Bibcode: 2006Natur.441..398P. — PMID 16724031.
- ↑ 1 2 Pennisi E. Genomics. DNA study forces rethink of what it means to be a gene (англ.) // Science : journal. — 2007. — June (vol. 316, no. 5831). — P. 1556—1557. — DOI:10.1126/science.316.5831.1556. — PMID 17569836.
- ↑ 1 2 Gericke, Niklas Markus; Hagberg, Mariana. Definition of historical models of gene function and their relation to students’ understanding of genetics (англ.) // Science & Education (англ.)русск. : journal. — 2006. — 5 December (vol. 16, no. 7—8). — P. 849—881. — DOI:
ru.wikipedia.org
Геном — Википедия
Гено́м — совокупность наследственного материала, заключённого в клетке организма[1]. Геном содержит биологическую информацию, необходимую для построения и поддержания организма. Большинство геномов, в том числе геном человека и геномы всех остальных клеточных форм жизни, построены из ДНК, однако некоторые вирусы имеют геномы из РНК[2].
Существует также и другое определение термина «геном», в котором под геномом понимают совокупность генетического материала гаплоидного набора хромосом данного вида[3][4]. Когда говорят о размерах генома эукариот, то подразумевают именно это определение генома, то есть размер эукариотического генома измеряют в парах нуклеотидов ДНК или пикограммах ДНК на гаплоидный геном[5].
У человека (Homo sapiens) наследственный материал соматической клетки представлен 23 парами хромосом (22 пары аутосом и пара половых хромосом), находящихся в ядре, а также клетка обладает множеством копий митохондриальной ДНК. Двадцать две аутосомы, половые хромосомы Х и Y, митохондриальная ДНК человека содержат вместе примерно 3,1 млрд пар оснований[1].
Термин «геном» был предложен Гансом Винклером в 1920 году в работе, посвящённой межвидовым амфидиплоидным растительным гибридам, для описания совокупности генов, заключённых в гаплоидном наборе хромосом организмов одного биологического вида. В Оксфордском энциклопедическом словаре указано, что термин образован слиянием слов «ген» и «хромосома»[6]. Однако Джошуа Ледерберг и Алекса T. МакКрэй считают, что ботаник Г. Винклер должен был быть знаком с ботаническими терминами «ризом», «таллом», «трахеом» и т. д. Все эти термины возникли до 20-х годов XX века, и суффикс «-ом» в них означает объединение частей в целое, например, «ризом» означает всю корневую систему растения. Таким образом, «геном» можно понимать как объединение генов в целое[7].
До недавнего времени термин «геном» использовался в двух смыслах. У эукариот геном соответствовал гаплоидному набору хромосом с локализованными в них генами. Генетики бактерий и вирусов употребляли термин «геном» для обозначения совокупности наследственных факторов одной хромосомы или группы сцепления прокариот. В генетике бактерий семантика термина «геном» претерпела дрейф в сторону обозначения всей наследственной конституции клетки, включая самые разные внехромосомные факультативные элементы. Постепенно в этом смысле термин «геном» стали употреблять и в генетике эукариот[8].
Первоначальный смысл этого термина указывал на то, что понятие генома, в отличие от генотипа, является генетической характеристикой вида в целом, а не отдельной особи. С развитием молекулярной генетики значение данного термина изменилось[9]. В настоящее время под «геномом» понимают совокупность наследственного материала отдельного представителя вида, примером может служить международный проект «1000 геномов»[en], целью которого является секвенирование геномов 1000 человек[10][11].
Геномы живых организмов — от вирусов до животных — различаются по размеру на шесть порядков: от нескольких тысяч пар оснований до нескольких миллиардов пар оснований. Если исключить вирусы, то для клеточных организмов ширина диапазона составит четыре порядка. По количеству генов диапазон значительно ýже и составляет четыре порядка с нижним пределом 2-3 гена у самых простых вирусов и с верхним значением около 40 тысяч генов у некоторых животных. Если исключить из рассмотрения вирусы и бактерии, которые ведут паразитический или симбиотический образ жизни, то диапазон изменчивости геномов по числу генов становится совсем узким, составляя немногим более одного порядка[12].
По соотношению размера генома и числа генов геномы могут быть разделены на два чётко выделенных класса:
- Небольшие компактные геномы размером, как правило, не более 10 млн пар оснований, со строгим соответствием между размером генома и числом генов. Такими геномами обладают все вирусы и прокариоты. У этих организмов плотность генов составляет от 0,5 до 2 генов на тысячу пар оснований, а между генами имеются очень короткие участки, занимающие 10-15 % длины генома. Межгенные участки в таких геномах состоят главным образом из регуляторных элементов. Помимо вирусов и прокариот, к этому классу могут быть отнесены и геномы большинства одноклеточных эукариот, хотя их геномы демонстрируют несколько меньшую зависимость между размером генома и числом генов, а размер генома может достигать 20 млн пар оснований.
- Обширные геномы размером более 100 млн пар оснований, у которых нет чёткой взаимосвязи между размером генома и числом генов. К этому классу относятся большие геномы многоклеточных эукариот и некоторых одноклеточных эукариот. В отличие от геномов первой группы, большинство нуклеотидов в геномах этого класса относится к последовательностям, которые не кодируют ни белков, ни РНК[13][14].
Прокариоты[править | править код]
Геном подавляющего числа прокариот представлен одиночной хромосомой, которая представляет собой кольцевую молекулу ДНК. Помимо хромосомы, в клетках бактерий часто находятся плазмиды — также замкнутые в кольцо ДНК, способные к независимой репликации[2]. У ряда бактерий, относящихся к различным филогенетическим группам, обнаружено линейное строение как хромосомы, так и плазмид. Например, геном спирохеты Borrelia burgdorferi, вызывающей болезнь Лайма, состоит из линейной хромосомы и нескольких плазмид, часть из которых имеет также линейное строение[15].
Геномы большинства прокариот маленькие и компактные, гены плотно упакованы и между ними находится минимальное количество регуляторной ДНК. Геномы почти всех эубактерий и архей содержат от 106 до 107 пар нуклеотидов и кодируют 1000–4000 генов[16]. Многие гены у прокариот организованы в совместно транскрибируемые группы — опероны[14].
Самыми маленькими геномами у прокариот обладают внутриклеточные симбионты и паразиты, такие как Hodgkinia cicadicola (144 Кб), Carsonella rudii (180 Кб)[17] или Mycoplasma genitalium (580 Кб)[18]. Самым большим прокариотическим геномом является геном обитающей в почве бактерии Sorangium cellulosum, размер которого составляет около 13 Мб[19].
Эукариоты[править | править код]
Практически вся генетическая информация у эукариот содержится в линейно-организованных хромосомах, находящихся в клеточном ядре. Внутриклеточные органеллы — митохондрии и хлоропласты — имеют свой собственный генетический материал. Геномы митохондрий и пластид организованы как прокариотические геномы.
Вирусы[править | править код]
Вирусные геномы очень малы. Например, геном вируса гепатита B представляет собой одну двуцепочечную кольцевую ДНК длиной около 3200 нуклеотидов [20].
Размер некоторых геномов с известной последовательностью[править | править код]
| Тип организма | Организм | Размер генома (пар оснований) |
Примерное число генов | Примечание | Ссылка на Genbank | |
|---|---|---|---|---|---|---|
| Вирус | Porcine circovirus тип 1 | 1,759 | 1.8 kb | Наименьший известный вирусный геном из способных самостоятельно размножаться в клетках эукариот.[21] | ||
| Вирус | Бактериофаг MS2 | 3 547 | 3.5 kb | 4 | Первый расшифрованный РНК-геном, 1976 год[22] | [1] |
| Вирус | SV40 | 5,224 | 5.2 kb | Расшифрован в 1978 году.[23] Миллионы людей были инфицированы вирусом SV40, так как в 1960-х годах он содержался в вакцине против вируса полиомиелита[24]. | ||
| Вирус | фаг Φ-X174 | 5,386 | 5.4 kb | 9 | Первый расшифрованный ДНК-геном, 1977 год.[25] | |
| Вирус | ВИЧ тип 2 | 10359 | 10.3 kb | 9 | [2] | |
| Вирус | лямбда (λ) фаг | 48,502 | 48.5 kb | Часто используется как вектор клонирования рекомбинантной ДНК.
[26][27][28] |
||
| Вирус | Мегавирус | 1,259,197 | 1.3 Mb | 1120 | До 2013 года — самый длинный из известных вирусных геномов.[29] | |
| Вирус | Pandoravirus salinus | 2,470,000 | 2.47 Mb | Самый длинный из известных вирусных геномов.[30] | ||
| Бактерия | Nasuia deltocephalinicola (штамм NAS-ALF) | 112,091 | 112 kb | 137 | Наименьший известный невирусный геном. Расшифрован в 2013 году.[31] | |
| Бактерия | Carsonella ruddii | 159,662 | 160 kb | |||
| Бактерия | Buchnera aphidicola | 600,000 | 600 kb | [32] | ||
| Бактерия | Wigglesworthia glossinidia | 700,000 | 700 kb | |||
| Бактерия | Haemophilus influenzae Гемофильная палочка | 1,830,000 | 1.8 Mb | Первый расшифрованный геном живого организма, июль 1995[33] Возбудитель гемофильной инфекции. | ||
| Бактерия | Escherichia coli | 4,600,000 | 4.6 Mb | 4288 | Наиболее хорошо изученная бактерия — E.Coli.[34] Широко используется в синтетической биологии. Часто применяется совместно с BioBrick. | |
| Бактерия | Solibacter usitatus (штамм Ellin 6076) | 9,970,000 | 10 Mb | [35] | ||
| Бактерия — цианобактерия | Prochlorococcus spp. (1.7 Mb) | 1,700,000 | 1.7 Mb | 1884 | Наименьший из известных геномов цианобактерий (способных к фотосинтезу). Один из морских видов цианобактерий.[36][37] | |
| Бактерия — цианобактерия | Nostoc punctiforme | 9,000,000 | 9 Mb | 7432 | Многоклеточная цианобактерия[38] | |
| Амёба | Polychaos dubium | 670,000,000,000 | 670 Gb | Возможно наибольший из известных геномов.[39] Оспаривается в 2010 году.[40] | ||
| Органелла эукариот | Митохондрия человека | 16,569 | 16.6 kb | [41] | ||
| Растение | Genlisea tuberosa, плотоядное цветное растение | 61,000,000 | 61 Mb | Наименьший известный на 2014 год геном цветочного растения.[42] | ||
| Растение | Arabidopsis thaliana | 135,000,000[43] | 135 Mb | 27,655[44] | Первый расшифрованный геном растения, декабрь 2000.[45] | |
| Растение | Populus trichocarpa | 480,000,000 | 480 Mb | 73013 | Первый расшифрованный геном дерева, сентябрь 2006[46] | |
| Растение | Fritillaria assyrica | 130,000,000,000 | 130 Gb | |||
| Растение | Paris japonica | 150,000,000,000 | 150 Gb | Наибольший из известных геном растения[47] | ||
| Растение — мох | Physcomitrella patens | 480,000,000 | 480 Mb | Первый из расшифрованных геномов мохообразных, январь 2008.[48] | ||
| Гриб — дрожжи | Saccharomyces cerevisiae | 12,100,000 | 12.1 Mb | 6294 | Первый из расшифрованных геномов эукариот, 1996[49] | |
| Гриб | Aspergillus nidulans | 30,000,000 | 30 Mb | 9541 | [50] | |
| Нематода | Pratylenchus coffeae | 20,000,000 | 20 Mb | [51]. Самый маленький из известных геном животного.[52] | ||
| Нематода | Caenorhabditis elegans (C.elegans) | 100,300,000 | 100 Mb | 19000 | Первый из расшифрованных геномов многоклеточного организма, декабрь 1998[53] | |
| Насекомое | Drosophila melanogaster (фруктовая мушка) | 175,000,000 | 175 Mb | 13600 | Размер зависит от штамма (175-180Mb; стандартный y w штамм 175Mb)[54] | |
| Насекомое | Apis mellifera (медовая пчела) | 236,000,000 | 236 Mb | 10157 | [55]) | |
| Насекомое | Bombyx mori Тутовый шелкопряд | 432,000,000 | 432 Mb | 14623 | [56] | |
| Насекомое | Solenopsis invicta (огненный муравей) | 480,000,000 | 480 Mb | 16569 | [57] | |
| Млекопитающее | Mus musculus (Домо́вая мышь) | 2,700,000,000 | 2.7 Gb | 20210 | [58] | |
| Млекопитающее | Homo sapiens (человек) | 3,289,000,000 | 3.3 Gb | 20000-30000 | Большая часть расшифрована одновременно Проектом Генома Человека и Celera Genomics Крейга Вентера в 2000 году. Окончательной датой расшифровки считают 2003 год.[59][60] | |
| Млекопитающее | Pan paniscus (Бонобо́ или Карликовый шимпанзе) | 3,286,640,000 | 3.3 Gb | 20000 | [61] | |
| Рыба | Tetraodon nigroviridis | 385,000,000 | 390 Mb | Наименьший из известных геномов позвоночных 340 Mb[62][63] — 385 Mb.[64] | ||
| Рыба | Protopterus aethiopicus | 130,000,000,000 | 130 Gb | Наибольший из известных геномов позвоночных | ||
- ↑ 1 2 Talking glossary of genetic terms: genome (англ.). National Human Genome Research Institute. Дата обращения 1 ноября 2012. Архивировано 4 ноября 2012 года.
- ↑ 1 2 Браун Т. А. Геномы = Genomes / /Пер. с англ. — М.-Ижевск: Институт компьютерных исследований, 2011. — 944 с. — ISBN 978-5-4344-0002-2.
- ↑ A Dictionary of genetics / R.C.King, W.D.Stansfield, P.K.Mulligan. — 7th. — Oxford University Press, 2006. — ISBN 13978-0-19-530762-7.
- ↑ Генетика: энциклопедический словарь / Картель Н. А., Макеева Е. Н., Мезенко А. М.. — Минск: Тэхналогія, 1999. — 448 с.
- ↑ Альбертс и др., 2013, с. 44.
- ↑ Oxford dictionaries: genome (англ.). OED. Дата обращения 13 ноября 2012. Архивировано 19 ноября 2012 года.
- ↑ Joshua Lederberg and Alexa T. McCray. ‘Ome Sweet ‘Omics — A Genealogical Treasury of Words (англ.) // The Scientist (англ.)русск. : journal. — 2001. — Vol. 15, no. 7. Архивировано 29 сентября 2006 года. Архивная копия от 29 сентября 2006 на Wayback Machine
- ↑ Голубовский М. Д. Век генетики: эволюция идей и понятий. Научно-исторические очерки. — СПб.: Борей Арт, 2000. — 262 с. — ISBN 5-7187-0304-3.
- ↑ Патрушев Л. И. Экспрессия генов / Ю. А. Берлин. — М.: Наука, 2000. — 526 с. — ISBN 5-02-001890-2.
- ↑ Abecasis G. R., Auton A., Brooks L. D., et al. An integrated map of genetic variation from 1,092 human genomes (англ.) // Nature : journal. — 2012. — November (vol. 491, no. 7422). — P. 56—65. — DOI:10.1038/nature11632. — PMID 23128226.
- ↑ Стартовал международный проект расшифровки геномов 1000 человек (неопр.). Membrana (24 января 2008). Дата обращения 13 ноября 2012.
- ↑ Кунин, 2014, с. 69.
- ↑ Кунин, 2014, с. 72.
- ↑ 1 2 Koonin E. V. Evolution of Genome Architecture (англ.) // Int J Biochem Cell Biol. Feb 2009; 41(2): 298–306.. — 2009. — Vol. 41, no. 2. — P. 298—306. — DOI:10.1016/j.biocel.2008.09.015.
- ↑ Fraser CM, Casjens S, Huang WM, et al. Genomic sequence of a Lyme disease spirochaete, Borrelia burgdorferi (англ.) // Nature. — 1997. — Vol. 390, no. 6660. — P. 580—586.
- ↑ Альбертс и др., 2013, с. 26.
- ↑ Koonin E. V., Wolf Y. I. Genomics of bacteria and archaea: the emerging dynamic view of the prokaryotic world (англ.) // Nucleic acids research. — 2008. — Vol. 36, no. 21. — P. 6688-6719.
- ↑ Альбертс и др., 2013, с. 27.
- ↑ Кунин, 2014, с. 134.
- ↑ Liang T. J. Hepatitis B: the virus and disease (англ.) // Hepatology (англ.)русск.. — Wiley-Liss, 2009. — Vol. 49, no. S5. — DOI:10.1002/hep.22881.
- ↑ Mankertz P. Molecular Biology of Porcine Circoviruses // Animal Viruses: Molecular Biology. — Caister Academic Press, 2008. — ISBN 978-1-904455-22-6.
- ↑ Fiers W; Contreras, R.; Duerinck, F.; Haegeman, G.; Iserentant, D.; Merregaert, J.; Min Jou, W.; Molemans, F.; Raeymaekers, A.; Van Den Berghe, A.; Volckaert, G.; Ysebaert, M. Complete nucleotide-sequence of bacteriophage MS2-RNA – primary and secondary structure of replicase gene (англ.) // Nature : journal. — 1976. — Vol. 260, no. 5551. — P. 500—507. — DOI:10.1038/260500a0. — Bibcode: 1976Natur.260..500F. — PMID 1264203.
- ↑ Fiers, W.; Contreras, R.; Haegeman, G.; Rogiers, R.; Van De Voorde, A.; Van Heuverswyn, H.; Van Herreweghe, J.; Volckaert, G.; Ysebaert, M. Complete nucleotide sequence of SV40 DNA (англ.) // Nature. — 1978. — Vol. 273, no. 5658. — P. 113—120. — DOI:10.1038/273113a0. — Bibcode: 1978Natur.273..113F. — PMID 205802.
- ↑ Le Page, Michael. Does SV40 contamination matter?, New Scientist (10 июня 2004). Дата обращения 29 марта 2010. «More than 40 years after SV40 was first discovered, in polio vaccine, these crucial questions remain fiercely controversial».
- ↑ Sanger, F.; Air, G.M.; Barrell, B.G.; Brown, N.L.; Coulson, A.R.; Fiddes, J.C.; Hutchison, C.A.; Slocombe, P. M.; Smith, M. Nucleotide sequence of bacteriophage phi X174 DNA (англ.) // Nature. — 1977. — Vol. 265, no. 5596. — P. 687—695. — DOI:10.1038/265687a0. — Bibcode: 1977Natur.265..687S. — PMID 870828.
- ↑ Thomason; Lynn; Court, Donald L.; Bubunenko, Mikail; Costantino, Nina; Wilson, Helen; Datta, Simanti; Oppenheim, Amos. Recombineering: genetic engineering in bacteria using homologous recombination (англ.) // Current Protocols in Molecular Biology : journal. — 2007. — Vol. Chapter 1. — P. Unit 1.16. — ISBN 0471142727. — DOI:10.1002/0471142727.mb0116s78. — PMID 18265390.
- ↑ Court; D. L.; Oppenheim, A. B.; Adhya, S. L. A new look at bacteriophage lambda genetic networks (англ.) // Journal of Bacteriology (англ.)русск. : journal. — 2007. — Vol. 189, no. 2. — P. 298—304. — DOI:10.1128/JB.01215-06. — PMID 17085553.
- ↑ Sanger; F.; Coulson, A.R.; Hong, G.F.; Hill, D.F.; Petersen, G.B. Nucleotide sequence of bacteriophage lambda DNA (англ.) // Journal of Molecular Biology (англ.)русск. : journal. — 1982. — Vol. 162, no. 4. — P. 729—773. — DOI:10.1016/0022-2836(82)90546-0. — PMID 6221115.
- ↑ Legendre, M; Arslan, D; Abergel, C; Claverie, J. M. Genomics of Megavirus and the elusive fourth domain of life| journal (англ.) // Communicative & Integrative Biology : journal. — 2012. — Vol. 5, no. 1. — P. 102—106. — DOI:10.4161/cib.18624. — PMID 22482024.
- ↑ Philippe, N.; Legendre, M.; Doutre, G.; Coute, Y.; Poirot, O.; Lescot, M.; Arslan, D.; Seltzer, V.; Bertaux, L.; Bruley, C.; Garin, J.; Claverie, J.-M.; Abergel, C. Pandoraviruses: Amoeba Viruses with Genomes Up to 2.5 Mb Reaching That of Parasitic Eukaryotes (англ.) // Science : journal. — 2013. — Vol. 341, no. 6143. — P. 281—286. — DOI:10.1126/science.1239181. — Bibcode: 2013Sci…341..281P. — PMID 23869018.
- ↑ Bennett, G. M.; Moran, N. A. Small, Smaller, Smallest: The Origins and Evolution of Ancient Dual Symbioses in a Phloem-Feeding Insect (англ.) // Genome Biology and Evolution (англ.)русск. : journal. — 2013. — 5 August (vol. 5, no. 9). — P. 1675—1688. — DOI:10.1093/gbe/evt118. — PMID 23918810.
- ↑ Shigenobu, S; Watanabe, H; Hattori, M; Sakaki, Y; Ishikawa, H. Genome sequence of the endocellular bacterial symbiont of aphids Buchnera sp. APS (англ.) // Nature : journal. — 2000. — 7 September (vol. 407, no. 6800). — P. 81—6. — DOI:10.1038/35024074. — PMID 10993077.
- ↑ Fleischmann R; Adams M; White O; Clayton R; Kirkness E; Kerlavage A; Bult C; Tomb J; Dougherty B; Merrick J; McKenney; Sutton; Fitzhugh; Fields; Gocyne; Scott; Shirley; Liu; Glodek; Kelley; Weidman; Phillips; Spriggs; Hedblom; Cotton; Utterback; Hanna; Nguyen; Saudek; Brandon. Whole-genome random sequencing and assembly of Haemophilus influenzae Rd (англ.) // Science : journal. — 1995. — Vol. 269, no. 5223. — P. 496—512. — DOI:10.1126/science.7542800. — Bibcode: 1995Sci…269..496F. — PMID 7542800.
- ↑ Frederick R. Blattner; Guy Plunkett III et al. The Complete Genome Sequence of Escherichia coli K-12 (англ.) // Science : journal. — 1997. — Vol. 277, no. 5331. — P. 1453—1462. — DOI:10.1126/science.277.5331.1453. — PMID 9278503.
- ↑ Challacombe, Jean F.; Eichorst, Stephanie A.; Hauser, Loren; Land, Miriam; Xie, Gary; Kuske, Cheryl R.; Steinke, Dirk. Biological Consequences of Ancient Gene Acquisition and Duplication in the Large Genome of Candidatus Solibacter usitatus Ellin6076 (англ.) // PLoS ONE (англ.)русск. : journal / Steinke, Dirk. — 2011. — 15 September (vol. 6, no. 9). — P. e24882. — DOI:10.1371/journal.pone.0024882. — Bibcode: 2011PLoSO…624882C. — PMID 21949776.
- ↑ Rocap, G.; Larimer, F. W.; Lamerdin, J.; Malfatti, S.; Chain, P.; Ahlgren, N. A.; Arellano, A.; Coleman, M.; Hauser, L.; Hess, W. R.; Johnson, Z. I.; Land, M.; Lindell, D.; Post, A. F.; Regala, W.; Shah, M.; Shaw, S. L.; Steglich, C.; Sullivan, M. B.; Ting, C. S.; Tolonen, A.; Webb, E. A.; Zinser, E. R.; Chisholm, S. W. Genome divergence in two Prochlorococcus ecotypes reflects oceanic niche differentiation (англ.) // Nature : journal. — 2003. — Vol. 424, no. 6952. — P. 1042—1047. — DOI:10.1038/nature01947. — Bibcode: 2003Natur.424.1042R. — PMID 12917642.
- ↑ Dufresne, A.; Salanoubat, M.; Partensky, F.; Artiguenave, F.; Axmann, I. M.; Barbe, V.; Duprat, S.; Galperin, M. Y.; Koonin, E. V.; Le Gall, F.; Makarova, K. S.; Ostrowski, M.; Oztas, S.; Robert, C.; Rogozin, I. B.; Scanlan, D. J.; De Marsac, N. T.; Weissenbach, J.; Wincker, P.; Wolf, Y. I.; Hess, W. R. Genome sequence of the cyanobacterium Prochlorococcus marinus SS120, a nearly minimal oxyphototrophic genome (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2003. — Vol. 100, no. 17. — P. 10020—10025. — DOI:10.1073/pnas.1733211100. — Bibcode: 2003PNAS..10010020D. — PMID 12917486.
- ↑ J. C.; Meeks; Elhai, J; Thiel, T; Potts, M; Larimer, F; Lamerdin, J; Predki, P; Atlas, R. An overview of the genome of Nostoc punctiforme, a multicellular, symbiotic cyanobacterium (англ.) // Drugs (англ.)русск. : journal. — Adis International, 2001. — Vol. 70, no. 1. — P. 85—106. — DOI:10.1023/A:1013840025518. — PMID 16228364.
- ↑ Parfrey LW; Lahr DJG; Katz L. A. The Dynamic Nature of Eukaryotic Genomes (англ.) // Molecular Biology and Evolution (англ.)русск. : journal. — Oxford University Press, 2008. — Vol. 25, no. 4. — P. 787—794. — DOI:10.1093/molbev/msn032. — PMID 18258610.
- ↑ ScienceShot: Biggest Genome Ever Архивировано 11 октября 2010 года., comments: «The measurement for Amoeba dubia and other protozoa which have been reported to have very large genomes were made in the 1960s using a rough biochemical approach which is now considered to be an unreliable method for accurate genome size determinations.»
- ↑ Anderson, S.; Bankier, A. T.; Barrell, B. G.; de Bruijn, M. H. L.; Coulson, A. R.; Drouin, J.; Eperon, I. C.; Nierlich, D. P.; Roe, B. A.; Sanger, F.; Schreier, P. H.; Smith, A. J. H.; Staden, R.; Young, I. G. Sequence and organization of the human mitochondrial genome (англ.) // Nature : journal. — 1981. — Vol. 290, no. 5806. — P. 457—465. — DOI:10.1038/290457a0. — Bibcode: 1981Natur.290..457A. — PMID 7219534.
- ↑ Fleischmann A; Michael TP; Rivadavia F; Sousa A; Wang W; Temsch EM; Greilhuber J; Müller KF; Heubl G. Evolution of genome size and chromosome number in the carnivorous plant genus Genlisea (Lentibulariaceae), with a new estimate of the minimum genome size in angiosperms (англ.) // Annals of Botany : journal. — 2014. — Vol. 114, no. 8. — P. 1651—1663. — DOI:10.1093/aob/mcu189. — PMID 25274549.
- ↑ TAIR — Genome Assembly
- ↑ Details — Arabidopsis thaliana — Ensembl Genomes 41
- ↑ Greilhuber J; Borsch T; Müller K; Worberg A; Porembski S; Barthlott W. Smallest angiosperm genomes found in Lentibulariaceae, with chromosomes of bacterial size (англ.) // Plant Biology : journal. — 2006. — Vol. 8, no. 6. — P. 770—777. — DOI:10.1055/s-2006-924101. — PMID 17203433.
- ↑ Tuskan G. A., Difazio S., Jansson S., Bohlmann J., Grigoriev I., Hellsten U., Putnam N., Ralph S., Rombauts S., Salamov A., Schein J., Sterck L., Aerts A., Bhalerao R. R., Bhalerao R. P., Blaudez D., Boerjan W., Brun A., Brunner A., Busov V., Campbell M., Carlson J., Chalot M., Chapman J., Chen G. L., Cooper D., Coutinho P. M., Couturier J., Covert S., Cronk Q., Cunningham R., Davis J., Degroeve S., Déjardin A., Depamphilis C., Detter J., Dirks B., Dubchak I., Duplessis S., Ehlting J., Ellis B., Gendler K., Goodstein D., Gribskov M., Grimwood J., Groover A., Gunter L., Hamberger B., Heinze B., Helariutta Y., Henrissat B., Holligan D., Holt R., Huang W., Islam-Faridi N., Jones S., Jones-Rhoades M., Jorgensen R., Joshi C., Kangasjärvi J., Karlsson J., Kelleher C., Kirkpatrick R., Kirst M., Kohler A., Kalluri U., Larimer F., Leebens-Mack J., Leplé J. C., Locascio P., Lou Y., Lucas S., Martin F., Montanini B., Napoli C., Nelson D. R., Nelson C., Nieminen K., Nilsson O., Pereda V., Peter G., Philippe R., Pilate G., Poliakov A., Razumovskaya J., Richardson P., Rinaldi C., Ritland K., Rouzé P., Ryaboy D., Schmutz J., Schrader J., Segerman B., Shin H., Siddiqui A., Sterky F., Terry A., Tsai C. J., Uberbacher E., Unneberg P., Vahala J., Wall K., Wessler S., Yang G., Yin T., Douglas C., Marra M., Sandberg G., Van de Peer Y., Rokhsar D. The genome of black cottonwood, Populus trichocarpa (Torr. & Gray) (англ.) // Science : journal. — 2006. — 15 September (vol. 313, no. 5793). — P. 1596—1604. — DOI:10.1126/science.1128691. — Bibcode: 2006Sci…313.1596T. — PMID 16973872.
- ↑ PELLICER, JAUME; FAY, MICHAEL F.; LEITCH, ILIA J. The largest eukaryotic genome of them all? (англ.) // Botanical Journal of the Linnean Society : journal. — 2010. — 15 September (vol. 164, no. 1). — P. 10—15. — DOI:10.1111/j.1095-8339.2010.01072.x.
- ↑ Lang D; Zimmer AD; Rensing SA; Reski R. Exploring plant biodiversity: the Physcomitrella genome and beyond (англ.) // Trends Plant Sci (англ.)русск. : journal. — 2008. — October (vol. 13, no. 10). — P. 542—549. — DOI:10.1016/j.tplants.2008.07.002. — PMID 18762443.
- ↑ Saccharomyces Genome Database (неопр.). Yeastgenome.org. Дата обращения 27 января 2011.
- ↑ Galagan J. E., Calvo S. E., Cuomo C., Ma L. J., Wortman J. R., Batzoglou S., Lee S. I., Baştürkmen M., Spevak C. C., Clutterbuck J., Kapitonov V., Jurka J., Scazzocchio C., Farman M., Butler J., Purcell S., Harris S., Braus G. H., Draht O., Busch S., D’Enfert C., Bouchier C., Goldman G. H., Bell-Pedersen D., Griffiths-Jones S., Doonan J. H., Yu J., Vienken K., Pain A., Freitag M., Selker E. U., Archer D. B., Peñalva M. A., Oakley B. R., Momany M., Tanaka T., Kumagai T., Asai K., Machida M., Nierman W. C., Denning D. W., Caddick M., Hynes M., Paoletti M., Fischer R., Miller B., Dyer P., Sachs M. S., Osmani S. A., Birren B. W. Sequencing of Aspergillus nidulans and comparative analysis with A. fumigatus and A. oryzae (англ.) // Nature : journal. — 2005. — Vol. 438, no. 7071. — P. 1105—1115. — DOI:10.1038/nature04341. — Bibcode: 2005Natur.438.1105G. — PMID 16372000.
- ↑ Leroy, S.; Bouamer, S.; Morand, S.; Fargette, M. Genome size of plant-parasitic nematodes (англ.) // Nematology (англ.)русск.. — Brill Publishers (англ.)русск., 2007. — Vol. 9. — P. 449—450. — DOI:10.1163/156854107781352089.
- ↑ Gregory TR. Animal Genome Size Database (неопр.). Gregory, T.R. (2016). Animal Genome Size Database. (2005).
- ↑ The C. elegans Sequencing Consortium. Genome sequence of the nematode C. elegans: a platform for investigating biology (англ.) // Science : journal. — 1998. — Vol. 282, no. 5396. — P. 2012—2018. — DOI:10.1126/science.282.5396.2012. — PMID 9851916.
- ↑ Ellis LL; Huang W; Quinn A. M. Intrapopulation Genome Size Variation in «Drosophila melanogaster» Reflects Life History Variation and Plasticity (англ.) // PLoS Genetics (англ.)русск. : journal. — 2014. — Vol. 10, no. 7. — P. e1004522. — DOI:10.1371/journal.pgen.1004522. — PMID 25057905.
- ↑ Honeybee Genome Sequencing Consortium; Weinstock; Robinson; Gibbs; Weinstock; Weinstock; Robinson; Worley; Evans; Maleszka; Robertson; Weaver; Beye; Bork; Elsik; Evans; Hartfelder; Hunt; Robertson; Robinson; Maleszka; Weinstock; Worley; Zdobnov; Hartfelder; Amdam; Bitondi; Collins; Cristino; Evans. Insights into social insects from the genome of the honeybee Apis mellifera (англ.) // Nature : journal. — 2006. — October (vol. 443, no. 7114). — P. 931—949. — DOI:
ru.wikipedia.org
Геном человека — Википедия
Геном человека — совокупность наследственного материала, заключённого в клетке человека. Человеческий геном состоит из 23 пар хромосом, находящихся в ядре, а также митохондриальной ДНК. Двадцать две аутосомы, две половые хромосомы Х и Y, а также митохондриальная ДНК человека содержат вместе примерно 3,1 млрд пар оснований[1].
В ходе выполнения проекта «Геном человека» была определена последовательность ДНК всех хромосом и митохондриальной ДНК. В настоящее время эти данные активно используются по всему миру в биомедицинских исследованиях. Полное секвенирование выявило, что человеческий геном содержит 20—25 тыс. активных генов[2], что значительно меньше, чем ожидалось в начале проекта (порядка 100 тыс.) — то есть только 1,5 % всего генетического материала кодирует белки или функциональные РНК. Остальная часть является некодирующей ДНК, которую часто называют мусорной ДНК[3], но которая, как оказалось, играет важную роль в регуляции активности генов и формирования всего организма в процессе развития[4][5].
Хромосомы[править | править код]
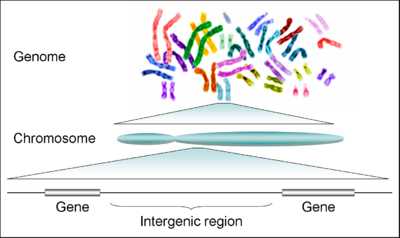 Геном человека состоит из 23 пар хромосом (в сумме 46 хромосом), где каждая хромосома содержит сотни генов, разделённых межгенным пространством. Межгенное пространство содержит регуляторные участки и ничего не кодирующую ДНК.
Геном человека состоит из 23 пар хромосом (в сумме 46 хромосом), где каждая хромосома содержит сотни генов, разделённых межгенным пространством. Межгенное пространство содержит регуляторные участки и ничего не кодирующую ДНК.
В геноме присутствует 23 пары хромосом: 22 пары аутосомных хромосом, а также пара половых хромосом X и Y. У человека мужской пол является гетерогаметным и определяется наличием Y хромосомы. Нормальные диплоидные соматические клетки имеют 46 хромосом[6][7].
Гены[править | править код]
Предварительные оценки предполагали наличие в геноме человека более 100 тысяч генов. По результатам проекта «Геном человека» количество генов, а точнее открытых рамок считывания, составило около 28 000 генов. В связи с усовершенствованием методов поиска (предсказания) генов предполагается дальнейшее уменьшение числа генов.
Число генов человека ненамного превосходит число генов у более простых организмов, например, круглого червя Caenorhabditis elegans или мухи Drosophila melanogaster. Так происходит из-за того, что в человеческом геноме широко представлен альтернативный сплайсинг. Альтернативный сплайсинг позволяет получить несколько различных белковых цепочек с одного гена. В результате человеческий протеом оказывается значительно больше протеома рассмотренных организмов. Большинство человеческих генов имеют множественные экзоны, и интроны часто оказываются значительно более длинными, чем граничные экзоны в гене.
Гены неравномерно распределены по хромосомам. Каждая хромосома содержит богатые и бедные генами участки. Эти участки коррелируют с хромосомными бендами (полосы поперёк хромосомы, которые видно в микроскоп) и с CG-богатыми участками. В настоящий момент значимость такого неравномерного распределения генов не вполне изучена.
Кроме генов, кодирующих белки, человеческий геном содержит тысячи РНК-генов, включая транспортную РНК (tRNA), рибосомную РНК, микроРНК и прочие не кодирующие белок РНК последовательности.
Регуляторные последовательности[править | править код]
В человеческом геноме найдено множество различных последовательностей, отвечающих за регуляцию гена. Под регуляцией понимается контроль экспрессии гена (процесс построения матричной РНК по участку молекулы ДНК). Обычно это короткие последовательности, находящиеся либо рядом с геном, либо внутри гена. Иногда они находятся на значительном расстоянии от гена (энхансеры). Систематизация этих последовательностей, понимание механизмов работы, а также вопросы взаимной регуляции группы генов группой соответствующих ферментов на текущий момент находятся только на начальной стадии изучения. Взаимная регуляция групп генов описывается с помощью сетей регуляции генов. Изучение этих вопросов находится на стыке нескольких дисциплин: прикладной математики, высокопроизводительных вычислений и молекулярной биологии. Знания появляются из сравнений геномов различных организмов и благодаря достижениям в области организации искусственной транскрипции гена в лабораторных условиях.
Идентификация регуляторных последовательностей в человеческом геноме частично была произведена на основе эволюционной консервативности (свойства сохранения важных фрагментов хромосомной последовательности, которые отвечают примерно одной и той же функции). Согласно некоторой гипотезе, в эволюционном дереве ветвь, разделяющая человека и мышь, появилась приблизительно 70-90 миллионов лет назад[8]. Для двух геномов компьютерными методами были выявлены консервативные последовательности (последовательности идентичные или очень слабо отличающиеся в сравниваемых геномах) в не кодирующей части и оказалось, что они активно участвуют в механизмах регуляции генов для обоих организмов[9].
Другой подход получения регуляторных последовательностей основан на сравнении генов человека и рыбы фугу. Последовательности генов и регуляторные последовательности у человека и рыбы фугу существенно схожи, однако геном рыбы фугу содержит в 8 раз меньший объём «мусорной ДНК». Такая «компактность» рыбьего генома позволяет значительно легче искать регуляторные последовательности для генов[10].
Прочие объекты в геноме[править | править код]
Кодирующие белок последовательности (множество последовательностей составляющих экзоны) составляют менее чем 1,5 % генома[3]. Не учитывая известные регуляторные последовательности, в человеческом геноме содержится масса объектов, которые выглядят как нечто важное, но функция которых, если она вообще существует, на текущий момент не выяснена. Фактически эти объекты занимают до 97 % всего объёма человеческого генома. К таким объектам относятся:
Представленная классификация не является исчерпывающей. Большая часть объектов вообще не классифицирована мировой научной общественностью на текущий момент.
Соответствующие последовательности, скорее всего, являются эволюционным артефактом. В современной версии генома их функция выключена, и на эти участки генома многие ссылаются как на «мусорную ДНК». Однако существует масса свидетельств, которая говорит о том, что эти объекты обладают некоторой функцией, которая не вполне понятна на текущий момент.
Псевдогены[править | править код]
Эксперименты с ДНК-микрочипами показали, что много участков генома, не являющихся генами, вовлечены в процесс транскрипции[11].
Вирусы[править | править код]
Около 1 % в геноме человека занимают встроенные гены ретровирусов (эндогенные ретровирусы). Эти гены обычно не приносят пользы хозяину, но существуют и исключения. Так, около 43 млн лет назад в геном предков обезьян и человека попали ретровирусные гены, служившие для построения оболочки вируса. У человека и обезьян эти гены участвуют в работе плаценты[12]. Большинство ретровирусов встроились в геном предков человека свыше 25 млн лет назад. Среди более молодых человеческих эндогенных ретровирусов полезных на настоящий момент не обнаружено[13][14].
Информационное содержание генома человека[править | править код]
Азотистые основания в ДНК (аденин, тимин, гуанин, цитозин) соответствуют 4 различным логическим состояниям, что эквивалентно 2 битам информации[15]. Таким образом, геном человека содержит более 6 гигабит информации в каждой цепи, что эквивалентно 800 мегабайтам и сопоставимо с количеством информации на компакт-диске[16]. Логика хранения данных в парных основаниях аналогична системе виртуализации данных RAID 1.
- ↑ Talking glossary of genetic terms: genome (англ.). National Human Genome Research Institute. Дата обращения 1 ноября 2012. Архивировано 4 ноября 2012 года.
- ↑ International Human Genome Sequencing Consortium. Finishing the euchromatic sequence of the human genome. (англ.) // Nature : journal. — 2004. — Vol. 431, no. 7011. — P. 931—945. [1]
- ↑ 1 2 International Human Genome Sequencing Consortium. Initial sequencing and analysis of the human genome. (англ.) // Nature : journal. — 2001. — Vol. 409, no. 6822. — P. 860—921. [2]
- ↑ «Мусорная» ДНК помогает включать гены (неопр.).
- ↑ «Мусорная» ДНК играет важнейшую роль в поддержании целостности генома (неопр.).
- ↑ Tjio J. H., Levan A. The chromosome number of man (неопр.) // Hereditas (англ.)русск.. — 1956. — Т. 42. — С. 1—6. Первая работа с точно установленным числом хромосом у человека.
- ↑ Human Chromosome Number, здесь рассказана история подсчёта хромосом у человека
- ↑ Nei M., Xu P., Glazko G. Estimation of divergence times from multiprotein sequences for a few mammalian species and several distantly related organisms. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2001. — Vol. 98, no. 5. — P. 2497—2502.
- ↑ Loots G., Locksley R., Blankespoor C., Wang Z., Miller W., Rubin E., Frazer K. Identification of a coordinate regulator of interleukins 4, 13, and 5 by cross-species sequence comparisons. (англ.) // Science : journal. — 2000. — Vol. 288, no. 5463. — P. 136—140. Summary
- ↑ Meunier, Monique Genoscope and Whitehead announce a high sequence coverage of the Tetraodon nigroviridis genome (англ.) (недоступная ссылка). Genoscope. Дата обращения 12 сентября 2006. Архивировано 20 августа 2002 года.
- ↑ Claverie J. Fewer genes, more noncoding RNA. (англ.) // Science. — 2005. — Vol. 309, no. 5740. — P. 1529—1530.
- ↑ Предки человека заимствовали полезные гены у вирусов
- ↑ Eugene D. Sverdlov. Retroviruses and primate evolution. BioEssays Volume 22, Issue 2, pages 161—171, February 2000
- ↑ Anders L Kjeldbjerg, Palle Villesen, Lars Aagaard, Finn Skou Pedersen. Gene conversion and purifying selection of a placenta-specific ERV-V envelope gene during simian evolution // BMC Evolutionary Biology. 2008. V. 8. P. 266.
- ↑ Деньгуб В. М., Смирнов В. Г. Единицы величин. Словарь-справочник. — М.: Издательство стандартов, 1990. — С. 25. — 240 с. — ISBN 5-7050-0118-5.
- ↑ How much information does human DNA store? — Quora
- Тарантул В. З. Геном человека. Энциклопедия, написанная четырьмя буквами. — Языки славянской культуры, 2003. — 396 с. — ISBN 5-94457-108-X.
- Ридли Мэтт. Геном: автобиография вида в 23 главах. — М.: Эксмо, 2008. — 432 с. — ISBN 5-699-30682-4
ru.wikipedia.org
Ген — это… Что такое Ген?
Ген (др.-греч. γένος — род) — структурная и функциональная единица наследственности живых организмов. Ген представляет собой последовательность ДНК, задающую последовательность определённого полипептида либо функциональной РНК. Гены (точнее, аллели генов) определяют наследственные признаки организмов, передающиеся от родителей потомству при размножении. При этом некоторые органеллы (митохондрии, пластиды) имеют собственную, определяющую их признаки, ДНК, не входящую в геном организма.
Среди некоторых организмов, в основном одноклеточных, встречается горизонтальный перенос генов, не связанный с размножением.
История термина
Термин «ген» был введён в употребление в 1909 году датским ботаником Вильгельмом Иогансеном три года спустя после введения Уильямом Бэтсоном термина «генетика». За сорок лет до появления понятия «ген» Чарльз Дарвин в 1868 году предложил «временную гипотезу» пангенеза, согласно которой все клетки организма отделяют от себя особые частицы или геммулы, а из них, в свою очередь, образуются половые клетки. Затем Гуго де Фриз в 1889 году, спустя 20 лет после Ч. Дарвина, выдвинул свою гипотезу внутриклеточного пангенеза и ввел термин «панген» для обозначения имеющихся в клетках материальных частиц, которые отвечают за вполне конкретные отдельные наследственные свойства, характерные для данного вида. Геммулы Ч. Дарвина представляли ткани и органы, пангены де Фриза соответствовали наследственным признакам внутри вида. Ещё через 20 лет В. Иогансен счёл удобным пользоваться только второй частью термина Гуго де Фриза «ген» и заменить им неопределенное понятие «зачатка», «детерминанта», «наследственного фактора». При этом В. Иогансен подчеркивал, что «этот термин совершенно не связан ни с какими гипотезами и имеет преимущество вследствие своей краткости и легкости, с которой его можно комбинировать с другими обозначениями». В. Иогансен сразу же образовал ключевое производное понятие «генотип» для обозначения наследственной конституции гамет и зигот в противоположность фенотипу[1].
Основные характеристики гена
Грегор МендельИзучением генов занимается наука генетика, родоначальником которой считается Грегор Мендель, который в 1865 году опубликовал результаты своих исследований о передаче по наследству признаков при скрещивании гороха. Сформулированные им закономерности впоследствии назвали Законами Менделя.
Среди учёных нет единого мнения под каким углом рассматривать ген. Одни учёные его рассматривают как информационную наследственную единицу, а единицей естественного отбора является вид, группа, популяция или отдельный индивид. Другие учёные, как например Ричард Докинз в своей книге «Эгоистичный ген», рассматривают ген как единицу естественного отбора, а сам организм — как машину для выживания генов.
В настоящее время, в молекулярной биологии установлено, что гены — это участки ДНК, несущие какую-либо целостную информацию — о строении одной молекулы белка или одной молекулы РНК. Эти и другие функциональные молекулы определяют развитие, рост и функционирование организма.
В то же время, каждый ген характеризуется рядом специфических регуляторных последовательностей ДНК (англ.)русск., таких как промоторы, которые принимают непосредственное участие в регулировании проявления гена. Регуляторные последовательности могут находиться как в непосредственной близости от открытой рамки считывания, кодирующей белок, или начала последовательности РНК, как в случае с промоторами (так называемые cis-регуляторные элементы, англ. cis-regulatory elements), так и на расстоянии многих миллионов пар оснований (нуклеотидов), как в случае с энхансерами, инсуляторами и супрессорами (иногда классифицируемые как trans-регуляторные элементы, англ. trans-regulatory elements). Таким образом, понятие гена не ограничено только кодирующим участком ДНК, а представляет собой более широкую концепцию, включающую в себя и регуляторные последовательности.
Изначально термин ген появился как теоретическая единица передачи дискретной наследственной информации. История биологии помнит споры о том, какие молекулы могут являться носителями наследственной информации. Большинство исследователей считали, что такими носителями могут быть только белки, так как их строение (20 аминокислот) позволяет создать больше вариантов, чем строение ДНК, которое составлено всего из четырёх видов нуклеотидов. Позже было экспериментально доказано, что именно ДНК включает в себя наследственную информацию, что было выражено в виде центральной догмы молекулярной биологии.
Гены могут подвергаться мутациям — случайным или целенаправленным изменениям последовательности нуклеотидов в цепи ДНК. Мутации могут приводить к изменению последовательности, а следовательно изменению биологических характеристик белка или РНК, которые, в свою очередь, могут иметь результатом общее или локальное изменённое или анормальное функционирование организма. Такие мутации в ряде случаев являются патогенными, так как их результатом является заболевание, или летальными на эмбриональном уровне. Однако, далеко не все изменения последовательности нуклеотидов приводят к изменению структуры белка (благодаря эффекту вырожденности генетического кода) или к существенному изменению последовательности и не являются патогенными. В частности, геном человека характеризуется однонуклеотидными полиморфизмами и вариациями числа копий (англ. copy number variations), такими как делеции и дупликации, которые составляют около 1 % всей нуклеотидной последовательности человека[2]. Однонуклеотидные полиморфизмы, в частности, определяют различные аллели одного гена.
Мономеры, составляющие каждую из цепей ДНК, представляют собой сложные органические соединения, включающие в себя азотистые основания: аденин(А) или тимин(Т) или цитозин(Ц) или гуанин(Г), пятиатомный сахар-пентозу-дезоксирибозу, по имени которой и получила название сама ДНК, а также остаток фосфорной кислоты. Эти соединения носят название нуклеотидов.
Гены и мимы
По аналогии с генами Ричардом Докинзом был введён в употребление термин «мим» — единица культурной информации. Если ген распространяется в химической среде, используя для размножения химические вещества, то мим распространяется в информационной среде: на носителях информации, в человеческой памяти, а также в сети. Также как гены конкурируют между собой за ресурсы: химические вещества, так и мимы конкурируют за информационное пространство. По целому ряду причин, между пространственным распределением генов и мимов могут наблюдаться достаточно жёсткие корреляции.
Свойства гена
- дискретность — несмешиваемость генов;
- стабильность — способность сохранять структуру;
- лабильность — способность многократно мутировать;
- множественный аллелизм — многие гены существуют в популяции во множестве молекулярных форм;
- аллельность — в генотипе диплоидных организмов только две формы гена;
- специфичность — каждый ген кодирует свой признак;
- плейотропия — множественный эффект гена;
- экспрессивность — степень выраженности гена в признаке;
- пенетрантность — частота проявления гена в фенотипе;
- амплификация — увеличение количества копий гена.
Классификация
- Структурные гены — уникальные компоненты генома, представляющие единственную последовательность, кодирующую определённый белок или некоторые виды РНК. (См. также статью гены домашнего хозяйства).
- Функциональные гены.
См. также
Примечания
- ↑ Голубовский М.Д. Век генетики: эволюция идей и понятий. Научно-исторические очерки. — СПб.: Борей Арт, 2000. — 262 с. — ISBN 5-7187-0304-3
- ↑ Levy S, Sutton G, Ng PC, Feuk L, Halpern AL, Walenz BP, Axelrod N, Huang J, Kirkness EF, Denisov G, Lin Y, Macdonald JR, Pang AW, Shago M, Stockwell TB, Tsiamouri A, Bafna V, Bansal V, Kravitz SA, Busam DA, Beeson KY, McIntosh TC, Remington KA, Abril JF, Gill J, Borman J, Rogers YH, Frazier ME, Scherer SW, Strausberg RL, Venter JC (2007). «The Diploid Genome Sequence of an Individual Human». PLoS Biol 5 (10): e254. PMID 17803354.
Ссылки
dic.academic.ru
Ген — Медицинская энциклопедия
I
(греч. genos род, происхождение)
структурно-функциональная единица генетического материала, наследственный фактор, который можно условно представить как отрезок молекулы ДНК (у некоторых вирусов — молекулы РНК), включающий нуклеотидную последовательность, в которой закодирована первичная структура полипептида (белка) либо молекулы транспортной или рибосомной РНК, синтез которых контролируется этим геном. Обусловливая первичную структуру конкретного белка, ген тем самым определяет формирование отдельного признака организма или клетки.
Предположение о существовании наследственных факторов впервые было высказано Менделем (G.J. Mendel) в 1865 г., который пришел к заключению, что передача признака от родителей потомству обусловлена передачей через половые клетки этих наследственных факторов, каждый из которых передается как нечто целое и независимое. В 1909 г. Иоганнсен (W. Johannsen) предложил обозначать менделевские наследственные факторы термином «гены». В 1911 г. Морганом (Th.Н. Morgan) и его сотрудниками было показано, что ген является участком хромосомы и что отдельная хромосома состоит из генов, последовательно расположенных по ее длине (см. Хромосомы). Каждый ген занимает свое определенное место (локус) на хромосоме. Позднее Морганом и его сотрудниками были созданы первые хромосомные карты, на которых они показали расположение отдельных генов на хромосомах. Совокупность хромосомных (или ядерных) генов, составляющих так называемый геном, и генов, локализованных в цитоплазматических структурах — митохондриях, пластидах, плазмидах, определяет генотип клетки или организма.
Ген может непосредственно определять наличие какого-либо признака (фена) организма или принимать участие в формировании нескольких признаков (явление плейотропии). Однако основная масса признаков у человека формируется в результате взаимодействия многих генов (явление полигении). Утрата гена или его изменение (см. Мутагенез) приводят к изменению признака, контролируемого этим геном. Степень проявления признака, контролируемого конкретным геном (экспрессивность гена), зависит также от условий окружающей среды. В то же время даже в пределах родственной группы особей, находящихся в сходных условиях существования, проявление одного и того же гена может варьировать по степени выраженности. Все это свидетельствует о том, что при формировании признаков генотип выступает как целостная система, функционирующая в строгой зависимости от внутриорганизменной и окружающей среды. Т.о., отдельный признак или совокупность всех признаков организма, т.е. его фенотип, являются результатом взаимодействия генотипа с окружающей средой; способность гена фенотипически проявлять себя тем или иным образом называют пенетрантностью гена.
У диплоидных организмов, т.е. у организмов, соматические клетки которых имеют двойной набор хромосом, гены представлены парой аллелей. Аллель — это одно из возможных состояний или один из возможных вариантов гена; теоретически число аллелей каждого гена неисчислимо, но не все они прошли эволюционный отбор. В гомологичных хромосомах аллельные гены расположены в гомологичных локусах. Аллельная пара генов может быть составлена из идентичных (явление гомозиготности) или различных (явление гетерозиготности) аллелей. У гетерозигот (организмов, аллельные гены которых различны) проявление одного аллеля на уровне признака организма (фенотипическое проявление) может полностью подавлять проявление другого аллеля. Подавляющий аллель называют доминантным, а подавляемый — рецессивным. Соответственно и контролируемые ими признаки носят название доминантных или рецессивных. Фенотипическое проявление рецессивных генов можно наблюдать только у тех организмов, которые оказываются гомозиготными в отношении такого рецессивного гена, т.е. оба аллельных гена у них рецессивны, или в случае, когда ген не имеет аллельной пары, например некоторые гены, расположенные на одной из половых хромосом при их XY-сочетании. У гетерозиготных организмов возможно и совместное (кодоминантное) проявление аллелей. Т.о., понятия «доминантный» и «рецессивный» отражают вклад данного гена в формирование конкретного признака. Свойство гена подавлять или быть подавленным в значительной мере зависит также от генного окружения — генотипической среды, в которой находится этот ген. Перенос гена в другое место хромосомы, влекущий за собой изменение его генного окружения, ведет к утрате этим геном своих свойств, в т.ч. даже такого свойства, выработанного в процессе длительной эволюции, как способность доминировать. Это явление называют эффектом положения гена. При возвращении гена в прежнее положение на хромосоме его способность доминировать восстанавливается.
Изучая механизмы регуляции функции гена, французские генетики Жакоб (F. Jacob) и Моно (J.L. Monod) пришли к заключению, что существуют структурные и регуляторные гены. К структурным генам относятся гены, которые контролируют (кодируют) первичную структуру матричных, или информационных, РНК, а через них последовательность аминокислот в синтезируемых полипептидах (см. Белки). Другую группу структурных генов составляют гены, определяющие последовательность нуклеотидов в полинуклеотидных цепях рибосомной РНК и транспортной РНК (см. Нуклеиновые кислоты).
Регуляторные гены контролируют синтез специфических веществ, так называемых ДНК-связывающих белков, которые регулируют активность структурных генов.
Используя способность некоторых Бактериофагов переносить фрагменты бактериальной хромосомы в другие бактериальные клетки (явление трансдукции), Беквит (J.R. Beckwith) и его сотрудники в 1969 г. впервые выделили, точно определили размер индивидуального гена кишечной палочки и получили его электронограмму. В 1967—1970 гг. Корана (Н.G. Khorana) осуществил химический синтез индивидуального гена.
По мере увеличения возможностей генетического анализа (см. Генетика) были получены все новые доказательства того, что ген, являясь функциональной единицей, вместе с тем имеет весьма сложное строение. Первые доказательства сложности организации гена получили в 1929 г. советские ученые А.С. Серебровский, Н.П. Дубинин и И.И. Агол.
Наряду со структурными и регуляторными генами в молекулах ДНК были обнаружены участки повторяющихся нуклеотидных последовательностей, функции которых не известны, а также мигрирующие нуклеотидные последовательности — так называемые мобильные гены. Найдены также псевдогены, представляющие собой неактивные копии известных генов, но расположенные в других частях генома.
В 1953 г. английский биохимик Крик (F. Н.С. Crick) и американский биохимик Уотсон (J.D. Watson) предложили модель строения молекулы ДНК и высказали предположение, вскоре полностью подтвердившееся, что последовательность нуклеотидов в полинуклеотидной цепи ДНК является кодом, в соответствии с которым осуществляется соединение аминокислотных остатков в полипептидной цепи белковых молекул, строящихся под контролем соответствующих генов. В дальнейшем этот генетический код был изучен более подробно. Было установлено, что включение одного аминокислотного остатка в строящуюся полипептидную цепь определяется сочетанием трех последовательно расположенных нуклеотидов, так называемых триплетов, причем включение одной и той же аминокислоты могут кодировать несколько различных триплетов Доказано, что генетический код универсален, т.е. он един для всех живых организмов. Реализация информации, «записанной» в гене, осуществляется с помощью посредника, которым является одна из разновидностей РНК — матричная, или информационная, РНК (мРНК). Синтез мРНК происходит на молекуле ДНК как на матрице. Такой матричный синтез обеспечивает точность «переписывания» (транскрипции) особенностей нуклеотидной последовательности гена на молекулу мРНК. Синтезированная мРНК из ядра клетки поступает в цитоплазму, где на рибосомах (см. Клетка) происходит реализация генетической информации (процесс трансляции), которая воплощается в последовательность аминокислот, соединяющихся в полипептидную цепь белка.
Средняя по размерам молекула белка содержит около 300 аминокислотных остатков. Следовательно, средний ген должен содержать не менее 1000—1500 нуклеотидов. Однако количество нуклеотидных пар в обычной молекуле ДНК по крайней мере в 10 раз превышает количество генов. Такая «избыточность» ДНК объясняется тем, что, например, у человека только 6—10% всей ДНК составляют кодирующие специфические нуклеотидные последовательности, остальные нуклеотиды в генетическом кодировании непосредственно не участвуют.
Большинство генов эукариот имеет прерывистую структуру: участок ДНК, кодирующий аминокислотную последовательность полипептидной цепи белка, разделен некодирующими вставками на несколько частей. Кроме того, некоторые некодирующие нуклеотидные последовательности обрамляют транскрибируемую единицу с концов. При транскрипции и те, и другие участки ДНК «считываются» в виде единой молекулы-предшественницы мРНК. Затем некодирующие участки выщепляются, а кодирующие участки соединяются друг с другом, образуя молекулу «зрелой» мРНК, способной транслироваться в молекулу белка. Другие некодирующие нуклеотидные последовательности могут играть роль сигнальных последовательностей, ответственных за начало определенных процессов в клетке. К ним относятся так называемые промоторы транскрипции, точки начала репликации ДНК, участки скручивания хромосом и др. Некодирующие последовательности состоят из множества семейств, характеризующихся разной степенью повторяемости нуклеотидов и различной организацией. Однако только немногие из этих последовательностей изучены настолько, чтобы определенной последовательности могла быть приписана определенная функция.
Т.о., ген представляет собой сложную микросистему, обеспечивающую жизнедеятельность клетки и организма в целом. Теория гена, постоянно углубляющаяся и развивающаяся, является основой генетической инженерии (Генетическая инженерия), конечной целью которой служит создание организмов с новыми наследственными свойствами, а также разработка способов лечения генетически обусловленных заболеваний (см. Наследственные болезни).
Библиогр.: Бочков Н.П. Генетика человека, М., 1978; Бочков Н.П., Захаров А.ф. и Иванов В.И. Медицинская генетика, М., 1984; Дубинин Н.П. Ген. БМЭ, 3-е изд., т. 5, с. 237, М., 1977; Льюин Б. Гены, пер. с англ., М., 1987.
II
(-ы) (греч. genos род, рождение, происхождение)
структурная и функциональная единица наследственности, контролирующая образование какого-либо признака, представляющая собой отрезок молекулы дезоксирибонуклеиновой кислоты (у некоторых вирусов — рибонуклеиновой кислоты).
Гены аллельные — см. Аллели.
Ген амбивалентный (лат. приставка ambi- вокруг, с обеих сторон + valens, valentis сильный) — Г., оказывающий как полезное, так и вредное действие на его носителя.
Ген аутосомный — Г., локализованный в любой хромосоме, за исключением половых.
Ген внехромосомный (син. Г. нехромосомный) — Г., локализованный вне хромосом в той или иной цитоплазматической структуре.
Ген главный — см. Олигоген.
Ген голандрический (греч. holos весь, полностью + anēr, andros мужчина) — Г., локализованный в участке Y-хромосомы, не имеющем гомологии в X-хромосоме, и поэтому абсолютно сцепленный с Y-хромосомой.
Ген гомеотический (греч. homoios подобный) — Г., действие которого обусловливает трансформацию эмбрионального зачатка одного органа в другой, возникающий обычно в несвойственном ему месте.
Гены гомодинамические — Г., контролирующие одновременно одни и те же процессы развития.
Гены гомологичные — Г. особей одного и того же биологического вида или разных видов с одинаковой функцией и локализацией относительно других генов.
Ген диагинический (греч. dia через + gynē женщина) — Г. X-хромосомы, переданной от матери к сыну.
Ген диандрический (греч. dia через + anēr, andros мужчина) — Г. X-хромосомы, переданной от отца к дочери.
Ген доминантный (лат. dominans, dominantis господствующий) — Г., сходно проявляющийся в гетеро- и гомозиготном состоянии и подавляющий проявление других аллелей этого гена.
Ген зависимый (син. Г. криптомерный — устар.) — Г., контролирующий при полигении образование специфического признака лишь во взаимодействии с другими неаллельными генами.
Ген идиоморфный (греч. idios своеобразный, необычный + morphē вид, форма) — Г., у которого один аллель заполняет всю популяцию, а все другие аллели вместе встречаются с частотой, не превышающей 1%.
Ген изоляционный — Г., в гетерозиготном состоянии обусловливающий снижение жизнеспособности или плодовитости особи.
Гены комбинационные — Г., детерминирующие различные процессы развития особи и образующие вторичный признак только путем комбинированного действия.
Гены компенсационные — как правило, рецессивные Г., взаимно изменяющие фенотипическое проявление друг друга.
Ген комплексный — Г., состоящий из частей, контролирующих один и тот же признак, не могущих быть разделенными при кроссинговере.
Гены комплементарные (лат. complementum дополнение) — неаллельные Г., каждый из которых может по-разному изменять один и тот же признак.
Ген, контролируемый полом (син. Г., модифицированный полом) — Г., присутствующий в генотипе обоих полов, но проявляющийся по-разному у особей мужского и женского пола.
Ген криптомерный (устар.; греч. kryptos скрытый + meros часть) — см. Ген зависимый.
Ген лабильный — Г., переходящий из одного стабильного состояния в другое через ряд мелких мутационных изменений.
Ген лабильный в развитии — Г., проявление которого сильно варьирует или отмечается не у всех особей.
Ген лабильный к среде — Г., проявление которого в значительной степени зависит от условий окружающей и внутренней среды.
Ген летальный — Г., обусловливающий гибель особи обычно до достижения ею половой зрелости.
Ген малый — см. Полиген.
Ген «межвидовой» — Г., детерминирующий межвидовые барьеры и не передающийся при межвидовом скрещивании.
Гены множественные — см. Гены полимерные.
Ген, модифицированный полом — см. Ген, контролируемый полом.
Ген мутабельный (лат. mutabilis изменчивый) — Г., отличающийся высокой частотой спонтанного мутирования.
Гены неаллельные — Г., занимающие неидентичные локусы хромосом.
Ген независимый — Г., в случае полигении способный самостоятельно детерминировать образование признака без участия других генов, контролирующих этот признак.
Ген нехромосомный — см. Ген внехромосомный.
Ген, ограниченный полом — Г., присутствующий у особей обоих полов, но фенотипически проявляющийся только у особей одного пола.
Ген плазмочувствительный — локализованный в хромосоме Г., проявление которого зависит от действия внехромосомных Г.
Ген плейотропный (греч. pleiōn более многочисленный + tropos направление) — Г., принимающий участие в формировании одновременно нескольких признаков.
Гены полимерные (греч. polymerēs состоящий из многих частей, множественный; син.: аддитивные факторы, Г. множественные, множественные факторы) — неаллельные Г., принимающие участие в формировании одного и того же признака.
Гены полипликатные (греч. poly- много + лат. plico, plicatum складывать) — идентичные пары Г. с одинаковым фенотипическим проявлением, но локализованные в разных хромосомах; различают дупликатные, трипликатные, квадрипликатные Г. и т.д., соответственно числу таких пар.
Ген полиургический (греч. poly- много + греч. ergon действие) — Г., вызывающий неодинаковый эффект в различных частях организма соответственно специфическим свойствам протоплазмы.
Ген регуляторный — Г., осуществляющий контроль активности оперона.
Ген рецессивный — Г., проявляющийся только в гомозиготном состоянии.
Ген сигнальный (син. ген-маркер) — Г. с известной локализацией и проявлением, используемый для картирования данной хромосомы.
Ген сложный — Г., состоящий из частей, не разделяемых кроссинговером, но обладающих независимой мутабельностью и частично независимых друг от друга.
Ген, стабильный в развитии — Г., характеризующийся регулярным и не варьирующим по силе проявлением.
Ген структурный (син. цистрон структурный) — Г., определяющий последовательность аминокислот в полипептидной цепи.
Ген, сцепленный с полом — Г., локализованный в половой хромосоме; различают Г., абсолютно и неполностью сцепленные с полом.
Гены цепные — группа Г., каждый из которых контролирует прохождение отдельного этапа в цепи реакций, обусловливающих в итоге образование признака.
Гены эквилокальные (лат. aequus равный, одинаковый + locus место, положение) — Г., занимающие идентичные участки гомологичных хромосом.
Ген эпистатический (греч. epistasis остановка, задержка) — см. Ген-ингибитор.
Источник: Медицинская энциклопедия на Gufo.me
Значения в других словарях
- Ген — (от греч. génos — род, происхождение) элементарная единица наследственности, представляющая отрезок молекулы дезоксирибонуклеиновой кислоты (См. Дезоксирибонуклеиновая кислота) — ДНК (у некоторых вирусов — рибонуклеиновой кислоты (См. Большая советская энциклопедия
- ген — Ген, гены, гена, генов, гену, генам, ген, гены, геном, генами, гене, генах Грамматический словарь Зализняка
- ГЕН — ГЕН (от греч. genos — род, происхождение) (наследственный фактор) — единица наследственного материала, ответственная за формирование какого-либо элементарного признака. У высших организмов (эукариот) входит в состав хромосом. Большой энциклопедический словарь
- ген — ГЕН (от греч. genos — род, происхождение), наследственный фактор, материальная единица наследственности, ответственная за формирование к.-л. элементарного признака. У высших организмов (эукариот) входит в состав хромосом. Совокупность всех… Сельскохозяйственный словарь
- ген — Материальный носитель наследственности, единица наследственной информации, способная к воспроизведению и расположенная в определенном локусе хромосомы. Обеспечивает преемственность в поколениях того или иного признака или свойства организма. Микробиология. Словарь терминов
- ГЕН — ГЕН, элемент, посредством которого наследственные свойства и особенности передаются из прколения в поколение у растений и животных. Это отрезок ДНК, который содержит определенные белки или пептиды (см. ГЕНЕТИЧЕСКИЙ код). Научно-технический словарь
- ген — Единица генетического материала; участок молекулы ДНК (у некоторых вирусов – РНК), определяющий (кодирующий) возможность развития какого-либо признака. Ген – функционально неделимая единица, т.е. Биология. Современная энциклопедия
- ген — ГЕН (от греч. genos — род, происхождение) участок молекулы ДНК (в некоторых случаях РНК), в котором закодирована информация о биосинтезе одной полипептидной цепи с определенной аминокислотной последовательностью. Г. — единица наследств. Химическая энциклопедия
- Ген — (греч. genos – происхождение). Структурная и функциональная единица наследственности, единица наследственной информации. Контролирует образование специфического признака. Представляет собой отрезок молекулы дезоксирибонуклеиновой или рибонуклеиновой кислоты. Толковый словарь психиатрических терминов
- ген — ГЕН см. Гены. Толковый словарь Кузнецова
- ген — ГЕН, гена, ·муж. (·греч. genos — род) (биол.). Предполагаемый зачаток наследственных свойств организма. Учение об устойчивых генах. Толковый словарь Ушакова
- ген — ГЕН — единица наследственнного вещества; локализованный участок хромосомы (локус), содержащий ДНК и обусловливающий передачу наследственной информации от клетки к клетке и ее реализацию путем синтеза информационной, матричной и рибосомальной РНК. Ботаника. Словарь терминов
- ген — см. гены. Малый академический словарь
- Ген — Последовательность цепочек ДНК, которые определяют порядок аминокислот в целом протеине или, иногда, в части протеина. Ген может состоять из сотен и тысяч цепочек ДНК, См. аллель. Физическая антропология
- ген — ГЕН Материальный носитель наследственности. Структурная и функциональная единица информации, способная к воспроизведению и расположенная в хромосоме. (Терминология спорта. Толковый словарь спортивных терминов, 2001) Словарь спортивных терминов
- ГЕН — ГЕН (от греч. genos — род, происхождение) — англ. gene; нем. Gen. Элементарная единица наследственности, посредством к-рой происходит «запись», хранение и передача наследственной информации от поколения к поколению. см. ГЕНЕТИКА, ГЕНОТИП, СОЦИОБИОЛОГИЯ. Социологический словарь
- ген — ген м. 1. Материальный носитель наследственности, находящийся в хромосомах клеточного ядра и участвующий в формировании признаков и свойств организма. 2. перен. Зародыш, зачаток. Толковый словарь Ефремовой
- ген — (от греч. genos — род, происхождение), наследственный фа ктор, функционально неделимая единица генетич. материала; участок молекулы ДНК (у нек-рых вирусов РНК), кодирующий первичную структуру полипептида… Биологический энциклопедический словарь
- ген — Гена, м. [греч. genos – род] (биол.). Материальный носитель наследственности, единица наследственной (генетической) информации, способная к воспроизведению и расположенная в определенном участке (локусе) данной хромосомы. Большой словарь иностранных слов
- ген — ГЕН, а, м. (спец.). Материальный носитель наследственности, единица наследственного материала, определяющая формирование элементарного признака в живом организме. Строение гена. | прил. генный, ая, ое и генетический, ая, ое. Толковый словарь Ожегова
- ген — сущ., кол-во синонимов: 14 аллель 3 ген-кандидат 1 ген-модификатор 1 ген-регулятор 1 ген-стартер 1 ген-супрессор 2 иммуноген 1 олигоген 1 онкоген 2 плазмаген 1 полиген 1 протоген 2 протоонкоген 1 супрессор 3 Словарь синонимов русского языка
- ген — Ген/. Морфемно-орфографический словарь
gufo.me
Ген — это… Что такое Ген?
структурно-функциональная единица генетического материала, наследственный фактор, который можно условно представить как отрезок молекулы ДНК (у некоторых вирусов — молекулы РНК), включающий нуклеотидную последовательность, в которой закодирована первичная структура полипептида (белка) либо молекулы транспортной или рибосомной РНК, синтез которых контролируется этим геном. Обусловливая первичную структуру конкретного белка, ген тем самым определяет формирование отдельного признака организма или клетки. Предположение о существовании наследственных факторов впервые было высказано Менделем (G.J. Mendel) в 1865 г., который пришел к заключению, что передача признака от родителей потомству обусловлена передачей через половые клетки этих наследственных факторов, каждый из которых передается как нечто целое и независимое. В 1909 г. Иоганнсен (W. Johannsen) предложил обозначать менделевские наследственные факторы термином «гены». В 1911 г. Морганом (Th.Н. Morgan) и его сотрудниками было показано, что ген является участком хромосомы и что отдельная хромосома состоит из генов, последовательно расположенных по ее длине (см. Хромосомы). Каждый ген занимает свое определенное место (локус) на хромосоме. Позднее Морганом и его сотрудниками были созданы первые хромосомные карты, на которых они показали расположение отдельных генов на хромосомах. Совокупность хромосомных (или ядерных) генов, составляющих так называемый геном, и генов, локализованных в цитоплазматических структурах — митохондриях, пластидах, плазмидах, определяет генотип клетки или организма. Ген может непосредственно определять наличие какого-либо признака (фена) организма или принимать участие в формировании нескольких признаков (явление плейотропии). Однако основная масса признаков у человека формируется в результате взаимодействия многих генов (явление полигении). Утрата гена или его изменение (см. Мутагенез) приводят к изменению признака, контролируемого этим геном. Степень проявления признака, контролируемого конкретным геном (экспрессивность гена), зависит также от условий окружающей среды. В то же время даже в пределах родственной группы особей, находящихся в сходных условиях существования, проявление одного и того же гена может варьировать по степени выраженности. Все это свидетельствует о том, что при формировании признаков генотип выступает как целостная система, функционирующая в строгой зависимости от внутриорганизменной и окружающей среды. Т.о., отдельный признак или совокупность всех признаков организма, т.е. его фенотип, являются результатом взаимодействия генотипа с окружающей средой; способность гена фенотипически проявлять себя тем или иным образом называют пенетрантностью гена. У диплоидных организмов, т.е. у организмов, соматические клетки которых имеют двойной набор хромосом, гены представлены парой аллелей. Аллель — это одно из возможных состояний или один из возможных вариантов гена; теоретически число аллелей каждого гена неисчислимо, но не все они прошли эволюционный отбор. В гомологичных хромосомах аллельные гены расположены в гомологичных локусах. Аллельная пара генов может быть составлена из идентичных (явление гомозиготности) или различных (явление гетерозиготности) аллелей. У гетерозигот (организмов, аллельные гены которых различны) проявление одного аллеля на уровне признака организма (фенотипическое проявление) может полностью подавлять проявление другого аллеля. Подавляющий аллель называют доминантным, а подавляемый — рецессивным. Соответственно и контролируемые ими признаки носят название доминантных или рецессивных. Фенотипическое проявление рецессивных генов можно наблюдать только у тех организмов, которые оказываются гомозиготными в отношении такого рецессивного гена, т.е. оба аллельных гена у них рецессивны, или в случае, когда ген не имеет аллельной пары, например некоторые гены, расположенные на одной из половых хромосом при их XY-сочетании. У гетерозиготных организмов возможно и совместное (кодоминантное) проявление аллелей. Т.о., понятия «доминантный» и «рецессивный» отражают вклад данного гена в формирование конкретного признака. Свойство гена подавлять или быть подавленным в значительной мере зависит также от генного окружения — генотипической среды, в которой находится этот ген. Перенос гена в другое место хромосомы, влекущий за собой изменение его генного окружения, ведет к утрате этим геном своих свойств, в т.ч. даже такого свойства, выработанного в процессе длительной эволюции, как способность доминировать. Это явление называют эффектом положения гена. При возвращении гена в прежнее положение на хромосоме его способность доминировать восстанавливается. Изучая механизмы регуляции функции гена, французские генетики Жакоб (F. Jacob) и Моно (J.L. Monod) пришли к заключению, что существуют структурные и регуляторные гены. К структурным генам относятся гены, которые контролируют (кодируют) первичную структуру матричных, или информационных, РНК, а через них последовательность аминокислот в синтезируемых полипептидах (см. Белки). Другую группу структурных генов составляют гены, определяющие последовательность нуклеотидов в полинуклеотидных цепях рибосомной РНК и транспортной РНК (см. Нуклеиновые кислоты). Регуляторные гены контролируют синтез специфических веществ, так называемых ДНК-связывающих белков, которые регулируют активность структурных генов. Используя способность некоторых Бактериофагов переносить фрагменты бактериальной хромосомы в другие бактериальные клетки (явление трансдукции), Беквит (J.R. Beckwith) и его сотрудники в 1969 г. впервые выделили, точно определили размер индивидуального гена кишечной палочки и получили его электронограмму. В 1967—1970 гг. Корана (Н.G. Khorana) осуществил химический синтез индивидуального гена. По мере увеличения возможностей генетического анализа (см. Генетика) были получены все новые доказательства того, что ген, являясь функциональной единицей, вместе с тем имеет весьма сложное строение. Первые доказательства сложности организации гена получили в 1929 г. советские ученые А.С. Серебровский, Н.П. Дубинин и И.И. Агол.Наряду со структурными и регуляторными генами в молекулах ДНК были обнаружены участки повторяющихся нуклеотидных последовательностей, функции которых не известны, а также мигрирующие нуклеотидные последовательности — так называемые мобильные гены. Найдены также псевдогены, представляющие собой неактивные копии известных генов, но расположенные в других частях генома.
В 1953 г. английский биохимик Крик (F. Н.С. Crick) и американский биохимик Уотсон (J.D. Watson) предложили модель строения молекулы ДНК и высказали предположение, вскоре полностью подтвердившееся, что последовательность нуклеотидов в полинуклеотидной цепи ДНК является кодом, в соответствии с которым осуществляется соединение аминокислотных остатков в полипептидной цепи белковых молекул, строящихся под контролем соответствующих генов. В дальнейшем этот генетический код был изучен более подробно. Было установлено, что включение одного аминокислотного остатка в строящуюся полипептидную цепь определяется сочетанием трех последовательно расположенных нуклеотидов, так называемых триплетов, причем включение одной и той же аминокислоты могут кодировать несколько различных триплетов Доказано, что генетический код универсален, т.е. он един для всех живых организмов. Реализация информации, «записанной» в гене, осуществляется с помощью посредника, которым является одна из разновидностей РНК — матричная, или информационная, РНК (мРНК). Синтез мРНК происходит на молекуле ДНК как на матрице. Такой матричный синтез обеспечивает точность «переписывания» (транскрипции) особенностей нуклеотидной последовательности гена на молекулу мРНК. Синтезированная мРНК из ядра клетки поступает в цитоплазму, где на рибосомах (см. Клетка) происходит реализация генетической информации (процесс трансляции), которая воплощается в последовательность аминокислот, соединяющихся в полипептидную цепь белка. Средняя по размерам молекула белка содержит около 300 аминокислотных остатков. Следовательно, средний ген должен содержать не менее 1000—1500 нуклеотидов. Однако количество нуклеотидных пар в обычной молекуле ДНК по крайней мере в 10 раз превышает количество генов. Такая «избыточность» ДНК объясняется тем, что, например, у человека только 6—10% всей ДНК составляют кодирующие специфические нуклеотидные последовательности, остальные нуклеотиды в генетическом кодировании непосредственно не участвуют. Большинство генов эукариот имеет прерывистую структуру: участок ДНК, кодирующий аминокислотную последовательность полипептидной цепи белка, разделен некодирующими вставками на несколько частей. Кроме того, некоторые некодирующие нуклеотидные последовательности обрамляют транскрибируемую единицу с концов. При транскрипции и те, и другие участки ДНК «считываются» в виде единой молекулы-предшественницы мРНК. Затем некодирующие участки выщепляются, а кодирующие участки соединяются друг с другом, образуя молекулу «зрелой» мРНК, способной транслироваться в молекулу белка. Другие некодирующие нуклеотидные последовательности могут играть роль сигнальных последовательностей, ответственных за начало определенных процессов в клетке. К ним относятся так называемые промоторы транскрипции, точки начала репликации ДНК, участки скручивания хромосом и др. Некодирующие последовательности состоят из множества семейств, характеризующихся разной степенью повторяемости нуклеотидов и различной организацией. Однако только немногие из этих последовательностей изучены настолько, чтобы определенной последовательности могла быть приписана определенная функция. Т.о., ген представляет собой сложную микросистему, обеспечивающую жизнедеятельность клетки и организма в целом. Теория гена, постоянно углубляющаяся и развивающаяся, является основой генетической инженерии (Генетическая инженерия), конечной целью которой служит создание организмов с новыми наследственными свойствами, а также разработка способов лечения генетически обусловленных заболеваний (см. Наследственные болезни). Библиогр.: Бочков Н.П. Генетика человека, М., 1978; Бочков Н.П., Захаров А.ф. и Иванов В.И. Медицинская генетика, М., 1984; Дубинин Н.П. Ген. БМЭ, 3-е изд., т. 5, с. 237, М., 1977; Льюин Б. Гены, пер. с англ., М., 1987.структурная и функциональная единица наследственности, контролирующая образование какого-либо признака, представляющая собой отрезок молекулы дезоксирибонуклеиновой кислоты (у некоторых вирусов — рибонуклеиновой кислоты).
Ген амбивале́нтный (лат. приставка ambi- вокруг, с обеих сторон + valens, valentis сильный) — Г., оказывающий как полезное, так и вредное действие на его носителя.
Ген аутосо́мный — Г., локализованный в любой хромосоме, за исключением половых.
Ген внехромосо́мный (син. Г. нехромосомный) — Г., локализованный вне хромосом в той или иной цитоплазматической структуре.Ген голандри́ческий (греч. holos весь, полностью + anēr, andros мужчина) — Г., локализованный в участке Y-хромосомы, не имеющем гомологии в X-хромосоме, и поэтому абсолютно сцепленный с Y-хромосомой.
Ген гомеоти́ческий (греч. homoios подобный) — Г., действие которого обусловливает трансформацию эмбрионального зачатка одного органа в другой, возникающий обычно в несвойственном ему месте.
Ге́ны гомодинами́ческие — Г., контролирующие одновременно одни и те же процессы развития.
Ге́ны гомологи́чные — Г. особей одного и того же биологического вида или разных видов с одинаковой функцией и локализацией относительно других генов.
Ген диагини́ческий (греч. dia через + gynē женщина) — Г. X-хромосомы, переданной от матери к сыну.
Ген диандри́ческий (греч. dia через + anēr, andros мужчина) — Г. X-хромосомы, переданной от отца к дочери.
Ген домина́нтный (лат. dominans, dominantis господствующий) — Г., сходно проявляющийся в гетеро- и гомозиготном состоянии и подавляющий проявление других аллелей этого гена.
Ген зави́симый (син. Г. криптомерный — устар.) — Г., контролирующий при полигении образование специфического признака лишь во взаимодействии с другими неаллельными генами.
Ген идиомо́рфный (греч. idios своеобразный, необычный + morphē вид, форма) — Г., у которого один аллель заполняет всю популяцию, а все другие аллели вместе встречаются с частотой, не превышающей 1%.Ген изоляцио́нный — Г., в гетерозиготном состоянии обусловливающий снижение жизнеспособности или плодовитости особи.
Ге́ны комбинацио́нные — Г., детерминирующие различные процессы развития особи и образующие вторичный признак только путем комбинированного действия.
Ге́ны компенсацио́нные — как правило, рецессивные Г., взаимно изменяющие фенотипическое проявление друг друга.
Ген ко́мплексный — Г., состоящий из частей, контролирующих один и тот же признак, не могущих быть разделенными при кроссинговере.
Ге́ны комплемента́рные (лат. complementum дополнение) — неаллельные Г., каждый из которых может по-разному изменять один и тот же признак.
Ген, контроли́руемый по́лом (син. Г., модифицированный полом) — Г., присутствующий в генотипе обоих полов, но проявляющийся по-разному у особей мужского и женского пола.
Ген криптоме́рный (устар.; греч. kryptos скрытый + meros часть) — см. Ген зависимый.
Ген лаби́льный — Г., переходящий из одного стабильного состояния в другое через ряд мелких мутационных изменений.
Ген лаби́льный в разви́тии — Г., проявление которого сильно варьирует или отмечается не у всех особей.
Ген лаби́льный к среде́ — Г., проявление которого в значительной степени зависит от условий окружающей и внутренней среды.
Ген лета́льный — Г., обусловливающий гибель особи обычно до достижения ею половой зрелости.
Ген «межвидово́й» — Г., детерминирующий межвидовые барьеры и не передающийся при межвидовом скрещивании.
Ге́ны мно́жественные — см. Гены полимерные.
Ген, модифици́рованный по́лом — см. Ген, контролируемый полом.
Ген мута́бельный (лат. mutabilis изменчивый) — Г., отличающийся высокой частотой спонтанного мутирования.
Ге́ны неалле́льные — Г., занимающие неидентичные локусы хромосом.
Ген незави́симый — Г., в случае полигении способный самостоятельно детерминировать образование признака без участия других генов, контролирующих этот признак.
Ген нехромосо́мный — см. Ген внехромосомный.
Ген, ограни́ченный по́лом — Г., присутствующий у особей обоих полов, но фенотипически проявляющийся только у особей одного пола.
Ген плазмочувстви́тельный — локализованный в хромосоме Г., проявление которого зависит от действия внехромосомных Г.
Ген плейотро́пный (греч. pleiōn более многочисленный + tropos направление) — Г., принимающий участие в формировании одновременно нескольких признаков.
Ге́ны полиме́рные (греч. polymerēs состоящий из многих частей, множественный; син.: аддитивные факторы, Г. множественные, множественные факторы) — неаллельные Г., принимающие участие в формировании одного и того же признака.Ге́ны полиплика́тные (греч. poly- много + лат. plico, plicatum складывать) — идентичные пары Г. с одинаковым фенотипическим проявлением, но локализованные в разных хромосомах; различают дупликатные, трипликатные, квадрипликатные Г. и т.д., соответственно числу таких пар.
Ген полиурги́ческий (греч. poly- много + греч. ergon действие) — Г., вызывающий неодинаковый эффект в различных частях организма соответственно специфическим свойствам протоплазмы.
Ген регулято́рный — Г., осуществляющий контроль активности оперона.
Ген рецесси́вный — Г., проявляющийся только в гомозиготном состоянии.
Ген сигна́льный (син. ген-маркер) — Г. с известной локализацией и проявлением, используемый для картирования данной хромосомы.
Ген сло́жный — Г., состоящий из частей, не разделяемых кроссинговером, но обладающих независимой мутабельностью и частично независимых друг от друга.
Ген, стаби́льный в разви́тии — Г., характеризующийся регулярным и не варьирующим по силе проявлением.
Ген структу́рный (син. цистрон структурный) — Г., определяющий последовательность аминокислот в полипептидной цепи.Ген, сце́пленный с по́лом — Г., локализованный в половой хромосоме; различают Г., абсолютно и неполностью сцепленные с полом.
Ге́ны цепны́е — группа Г., каждый из которых контролирует прохождение отдельного этапа в цепи реакций, обусловливающих в итоге образование признака.
Ге́ны эквилока́льные (лат. aequus равный, одинаковый + locus место, положение) — Г., занимающие идентичные участки гомологичных хромосом.
Ген эпистати́ческий (греч. epistasis остановка, задержка) — см. Ген-ингибитор.dic.academic.ru
как это было и как это будет
Это было семь лет назад — 26-го июня 2000 года. На совместной пресс-конференции с участием президента США и премьер-министра Великобритании представители двух исследовательских групп — International Human Genome Sequencing Consortium (IHGSC) и Celera Genomics — объявили о том, что работы по расшифровке генома человека, начавшиеся ещё в 70-х годах, успешно завершены, и черновой его вариант составлен. Начался новый эпизод развития человечества — постгеномная эра.
Что может дать нам расшифровка генома, и стоят ли потраченные средства и усилия достигнутого результата? Фрэнсис Коллинз (Francis S. Collins), руководитель американской программы «Геном человека», в 2000 году дал следующий прогноз развития медицины и биологии в постгеномную эру:
- 2010 год — генетическое тестирование, профилактические меры, снижающие риск заболеваний, и генная терапия до 25 наследственных заболеваний. Медсёстры начинают выполнять медико-генетические процедуры. Широко доступна преимплантационная диагностика, активно обсуждаются ограничения в применении данного метода. В США приняты законы для предотвращения генетической дискриминации и соблюдения конфиденциальности. Практические приложения геномики доступны не всем, особенно это чувствуется в развивающихся странах.
- 2020 год — на рынке появляются лекарства от диабета, гипертонии и других заболеваний, разработанные на основе геномной информации. Разрабатывается терапия рака, прицельно направленная на свойства раковых клеток определенных опухолей. Фармакогеномика становится общепринятым подходом для создания многих лекарств. Изменение способа диагностики психических заболеваний, появление новых способов их лечения, изменение отношения общества к таким заболеваниям. Практические приложения геномики все еще доступны далеко не везде.
- 2030 год — определение последовательности нуклеотидов всего генома отдельного индивида станет обычной процедурой, стоимость которой менее $1000. Каталогизированы гены, участвующие в процессе старения. Проводятся клинические испытания по увеличению максимальной продолжительности жизни человека. Лабораторные эксперименты на человеческих клетках заменены экспериментами на компьютерных моделях. Активизируются массовые движения противников передовых технологий в США и других странах.
- 2040 год — Все общепринятые меры здравоохранения основаны на геномике. Определяется предрасположенность к большинству заболеваний (ещё до рождения). Доступна эффективная профилактическая медицина с учетом особенностей индивида. Болезни определяются на ранних стадиях путем молекулярного мониторинга.
Для многих заболеваний доступна генная терапия. Замена лекарств продуктами генов, вырабатываемыми организмом при ответе на терапию. Средняя продолжительность жизни достигнет 90 лет благодаря улучшению социо-экономических условий. Проходят серьезные дебаты о возможности человека контролировать собственную эволюцию.
Неравенство в мире сохраняется, создавая напряженность на международном уровне.
Как видно из прогноза, геномная информация в недалеком будущем может стать основой лечения и профилактики множества болезней. Без информации о своих генах (а она умещается на стандарный DVD-диск) человек в будущем сможет вылечить разве что насморк у какого-нибудь целителя в джунглях. Это кажется фантастикой? Но когда-то такой же фантастикой была поголовная вакцинация от оспы или интернет (заметьте, в 70-х его еще не существовало)! В будущем генетический код ребенка будут выдавать родителям в роддоме. Теоретически, при наличии такого диска, лечение и предотвращение любых недугов отдельно взятого человека станет сущим пустяком. Профессиональный врач сможет в предельно сжатые сроки поставить диагноз, назначить эффективное лечение, и даже определить вероятность появления разных болезней в будущем. К примеру, современные генетические тесты уже позволяют точно определить степень предрасположенности женщины к раку груди. Почти наверняка, лет через 40–50 ни один уважающий себя врач без генетического кода не захочет «лечить вслепую» — подобно тому, как сегодня хирургия не может обойтись без рентгеновского снимка.
Давайте зададимся вопросом — а достоверно ли сказанное, или, может быть, в действительности всё будет наоборот? Смогут ли люди наконец победить все болезни и придут ли они ко всеобщему счастью? Увы. Начнем с того, что Земля маленькая, и счастья на всех не хватит. По правде сказать, его не хватит даже для половины населения развивающихся стран. «Счастье» предназначено в основном для государств, развитых в плане науки, в частности — наук биологических. Например методика, с помощью которой можно «прочесть» генетический код любого человека, уже давно запатентована. Это отлично отработанная автоматизированная технология — правда, дорогостоящая и очень тонкая. Хочешь, покупай лицензию, а хочешь — придумывай новую методику. Только вот денег на подобную разработку хватит далеко не у всех стран! В итоге ряд государств будет обладать медициной, существенно опережающей уровень остального мира. Естественно, в слаборазвитых странах Красным Крестом будут строиться благотворительные больницы, госпитали и геномные центры. И постепенно это приведет к тому, что генетическая информация пациентов развивающихся стран (которых большинство), сосредоточится у двух-трех держав, финансирующих эту благотворительность. Что можно сделать, имея такую информацию — даже представить трудно. Может, и ничего страшного. Однако возможен и другой исход. Битва за приоритет, сопровождавшая секвенирование генома, наглядно подтверждает важность доступности генетической информации. Давайте кратко вспомним некоторые факты из истории программы «Геном человека».
Противники расшифровки генома считали поставленную задачу нереальной, ведь ДНК человека в десятки тысяч раз длиннее молекул ДНК вирусов или плазмид. Главный аргумент против был: «проект потребует миллиарды долларов, которых недосчитаются другие области науки, поэтому геномный проект затормозит развитие науки в целом. А если все-таки деньги найдутся и геном человека будет расшифрован, то полученная в результате информация не оправдает затрат…» Однако Джеймс Уотсон, один из первооткрывателей структуры ДНК и идеолог программы тотального прочтения генетической информации, остроумно парировал: «лучше не поймать большую рыбу, чем не поймать маленькую» [1], [2]. Аргумент учёного был услышан — проблему генома вынесли на обсуждение в конгресс США, и в итоге была принята национальная программа «Геном человека».
В американском городе Бетесда, что недалеко от Вашингтона, находится один из координационных центров HUGO (HUman Genome Organization). Центр координирует научную работу по теме «Геном человека» в шести странах — Германии, Англии, Франции, Японии, Китае и США. В работу включились учёные из многих стран мира, объединенные в три команды: две межгосударственные — американская Human Genome Project и британская из Wellcome Trust Sanger Institute — и частная корпорация из штата Мериленд, включившаяся в игру чуть позже, — Celera Genomics. Кстати, это пожалуй первый случай в биологии, когда на таком высоком уровне частная фирма соревновалась с межгосударственными организациями.
Борьба происходила с использованием колоссальных средств и возможностей. Как отмечали некоторое время назад российские эксперты, Celera стояла на плечах у программы «Геном Человека», то есть использовала то, что уже было сделано в рамках глобального проекта. Действительно, Celera Genomics подключилась к программе не сначала, а когда проект уже шёл полным ходом. Однако специалисты из Celera усовершенствовали алгоритм секвенирования. Кроме того, по их заказу был построен суперкомпьютер, который позволял складывать выявляемые «кирпичики» ДНК в результирующую последовательность быстрее и точнее. Конечно, все это не давало компании Celera безоговорочного преимущества, однако считаться с ней как с полноправным участником гонки заставило.
Появление Celera Genomics резко повысило напряженность — те, кто был занят в государственных программах, почувствовали жёсткую конкуренцию. Кроме того, после создания компании остро встал вопрос об эффективности использования государственных капиталовложений. Во главе Celera стал профессор Крейг Вентер (Craig Venter) [3], который имел огромный опыт научной работы по государственной программе «Геном человека». Именно он и заявил, что все публичные программы малоэффективны и что в его фирме геном секвенируют быстрее и дешевле. А тут появился ещё один фактор — спохватились крупные фармацевтические компании. Дело в том, что если вся информация о геноме окажется в открытом доступе, они лишатся интеллектуальной собственности, и нечего будет патентовать. Озабоченные этим, они вложили миллиарды долларов в Celera Genomics (с которой, вероятно, было проще договориться). Это еще более укрепило её позиции. В ответ на это коллективам межгосударственного консорциума срочно пришлось повышать эффективность работ по расшифровке генома. Сначала работа шла несогласованно, но потом были достигнуты определенные формы сосуществования — и гонка начала наращивать темп.
Финал был красивым — конкурирующие организации по взаимной договоренности одновременно объявили о завершении работ по расшифровке генома человека [4], [5]. Произошло это, как мы уже писали — 26 июня 2000 года. Но разница во времени между Америкой и Англией вывела на первое место США.

Рисунок 1. «Гонка за генóм», в которой участвовали межгосударственная и частная компании, формально завершилась «ничьей»: обе группы исследователей опубликовали свои достижения практически одновременно. Руководитель частной компании Celera Genomics Крейг Вентер опубликовал свою работу в журнале Science в соавторстве с ~270 учёными, работавшими под его началом [5]. Работа, выполненная международным консорциумом по секвенированию человеческого генома (IHGSC), опубликована в журнале Nature, и полный список авторов насчитывает около 2800 человек, работавших в почти трёх десятках центров по всему миру [4].
Исследования в сумме продлились 15 лет. Создание первого «чернового» варианта генома человека обошлось в 300 миллионов долларов. Однако на все исследования по этой теме, включая сравнительные анализы и решение ряда этических проблем, было выделено в сумме около трех миллиардов долларов. Celera Genomics вложила примерно столько же, правда, она истратила их всего за шесть лет. Цена колоссальная, но эта сумма ничтожна в сравнении с той выгодой, которую получит страна-разработчик от ожидаемой вскоре окончательной победы над десятками серьезных заболеваний. В начале октября 2002 года в интервью «Ассошиэйтед пресс» президент Celera Genomics Крейг Вентер заявил, что одна из его некоммерческих организаций планирует заняться изготовлением компакт-дисков, содержащих максимум информации о ДНК клиента. Предварительная стоимость такого заказа — более 700 тысяч долларов. А одному из первооткрывателей структуры ДНК — доктору Джеймсу Уотсону — уже в этом году были подарены два DVD-диска с его геномом общей стоимостью 1 млн. долларов [6], — как видим, цены падают. Так, вице-президент фирмы 454 Life Sciences Майкл Эгхолм (Michael Egholm) сообщил, что в скором времени компания сможет довести цену расшифровки до 100 тыс. долларов.
Широкая известность и масштабное финансирование — палка о двух концах. С одной стороны, за счет неограниченных средств работа продвигается легко и быстро. Но с другой стороны, результат исследований должен получиться таким, каким его заказывают. К началу 2001 года в геноме человека со стопроцентной достоверностью было идентифицировано больее 20 тыс. генов. Эта цифра оказалось в три раза меньше, чем было предсказано всего за два года до этого. Вторая команда исследователей из Национального института геномных исследований США во главе с Френсисом Коллинсом независимым способом получила те же результаты — между 20 и 25 тыс. генов в геноме каждой человеческой клетки. Однако неопределенность в окончательные оценки внесли два других международных совместных научных проекта. Доктор Вильям Хезелтайн (руководитель фирмы Human Genome Studies) настаивал, что в их банке содержится информация о 140 тыс. генов. И этой информацией он не собирается пока делиться с мировой общественностью. Его фирма вложила деньги в патенты и собирается зарабатывать на полученной информации, поскольку она относится к генам широко распространенных болезней человека. Другая группа заявила о 120 тыс. идентифицированных генов человека и также настаивала, что именно эта цифра отражает общее число генов человека.
Тут необходимо уточнить, что эти исследователи занимались расшифровкой последовательности ДНК не самого генома, а ДНК-копий информационных (называемых также матричными) РНК (иРНК или мРНК). Другими словами, исследовался не весь геном, а только та его часть, что перекодируется клеткой в мРНК и направляет синтез белков. Поскольку один ген может служить матрицей для производства нескольких различных видов мРНК (что определяется многими факторами: тип клетки, стадия развития организма и т. д.), то и суммарное число всех различных последовательностей мРНК (а это именно то, что запатентовала Human Genome Studies) будет значительно бóльшим. Скорее всего, использовать это число для оценки количества генов в геноме просто некорректно.
Очевидно, что наспех «приватизированная» генетическая информация будет в ближайшие годы тщательно проверяться, пока точное число генов станет, наконец, общепринятым. Но настораживает тот факт, что в процессе «познания» патентуется вообще все, что только можно запатентовать. Тут даже не шкура не убитого медведя, а вообще все, что находилось в берлоге, было поделено! Кстати, на сегодня дебаты сбавили обороты, и геном человека официально насчитывает только 21667 генов (версия NCBI 35, датированная октябрём 2005 года). Следует отметить, что пока большая часть информации всё-таки остаётся общедоступной. Сейчас существуют базы данных, в которых аккумулирована информация о структуре генома не только человека, но и геномов многих других организмов (например, EnsEMBL). Однако попытки получить исключительные права на использование каких-либо генов или последовательностей в коммерческих целях всегда были, есть сейчас и будут предприниматься впредь.
На сегодня основные цели структурной части программы уже в основном выполнены — геном человека почти полностью прочитан. Первый, «черновой» вариант последовательности, опубликованный в начале 2001 года [4], был далек от совершенства. В нём отсутствовало приблизительно 30% последовательности генома в целом, из них около 10% последовательности так называемого эухроматина — богатых генами и активно экспрессирующихся участков хромосом. Согласно последним подсчётам, эухроматин составляет примерно 93,5% от всего генома [7]. Оставшиеся же 6,5% приходятся на гетерохроматин — эти участки хромосом бедны генами и содержат большое количество повторов, которые представляют серьезные трудности для ученых, пытающихся прочесть их последовательность [8]. Более того, считается, что ДНК в гетерохроматине находится в неактивном состоянии и не экспрессируется. (Этим можно объяснить такое «невнимание» ученых к оставшимся «малым» процентам человеческого генома.) Но даже имевшиеся на 2001 год «черновые» варианты эухроматиновых последовательностей содержали большое количество разрывов, ошибок и неверно соединенных и ориентированных фрагментов. Нисколько не умаляя значения для науки и ее приложений появление этого «черновика», стоит однако отметить, что использование этой предварительной информации в крупномасштабных экспериментах по анализу генома в целом (например, при исследовании эволюции генов или общей организации генома) выявило множество неточностей и артефактов. Поэтому дальнейшая и не менее кропотливая работа, «последние вершки», была абсолютно необходима.

Рисунок 2. Слева: Автоматизированная линия подготовки образцов ДНК для секвенирования в Центре Геномных исследований института Уайтхеда. Справа: Лаборатория в Сэнгеровском институте, заполненная автоматами для высокопроизводительной расшифровки последовательностей ДНК.
Завершение расшифровки заняло еще несколько лет и привело почти что к удвоению стоимости всего проекта. Однако уже в 2004 г. было объявлено, что эухроматин прочитан на 99% с общей точностью одна ошибка на 100 000 пар оснований. Количество разрывов уменьшилось в 400 раз. Аккуратность и полнота прочтения стала достаточной для эффективного поиска генов, отвечающих за то или иное наследственное заболевание (например, диабет или рак груди). Практически это означает, что исследователям больше не надо заниматься трудоемким подтверждением последовательностей генов, с которыми они работают, так как можно полностью положиться на определенную и доступную каждому последовательность всего генома.
Таким образом, изначальный план проекта был значительно перевыполнен. Помогло ли это нам в понимании того, как устроен и работает наш геном? Безусловно. Авторы статьи в Nature, в которой был опубликован «окончательный» (на 2004 год) вариант генома [7], провели с его использованием несколько анализов, которые были бы абсолютно бессмысленны, имей они на руках только «черновую» последовательность. Оказалось, что более тысячи генов «родились» совсем недавно (по эволюционным меркам, конечно) — в процессе удвоения исходного гена и последующего независимого развития дочернего гена и гена-родителя. А чуть меньше сорока генов недавно «умерли», накопив мутации, сделавшие их совершенно неактивными. Другая статья, вышедшая в том же номере журнала Nature, прямо указывает на недостатки метода, использованного учеными из Celera [9]. Следствием этих недостатков стали пропуски многочисленных повторов в прочитанных последовательностях ДНК и, как результат, недооценённая длина и сложность всего генома. Чтобы не повторять подобных ошибок в будущем, авторы статьи предложили использовать гибридную стратегию — комбинацию высокоэффективного подхода, использовавшегося учеными из Celera, и сравнительно медленного и трудоемкого, но и более надежного метода, применявшегося исследователями из IHGSC.
Куда дальше будет направлено беспрецедентное исследование «Геном человека»? Кое-что об этом можно сказать уже сейчас. Основанный в сентябре 2003 года международный консорциум ENCODE (ENCyclopaedia Of DNA Elements) поставил своей целью обнаружение и изучение «управляющих элементов» (последовательностей) в геноме человека. Действительно, ведь 3 млрд. пар оснований (а именно такова длина генома человека) содержат всего лишь 22 тыс. генов, разбросанных в этом океане ДНК непонятным для нас образом. Что управляет их экспрессией? Зачем нам такой избыток ДНК? Действительно ли он является балластом, или же все-таки проявляет себя, обладая какими-то неизвестными функциями [10]?
Для начала, в качестве пилотного проекта, ученые из ENCODE «пристально вгляделись» в последовательность, составляющую 1% от генома человека (30 млн. пар оснований), используя новейшее оборудование для исследований в молекулярной биологии. Результаты были опубликованы в апреле нынешнего года в Nature [11]. Оказалось, что бóльшая часть генома человека (в том числе участки, считавшиеся ранее «молчащими») служит матрицей для производства различных РНК, многие из которых не являются информационными, поскольку не кодируют белков. Многие из этих «некодирующих» РНК перекрываются с «классическими» генами (участками ДНК, кодирующими белки). Неожиданным результатом было и то, как регуляторные участки ДНК были расположены относительно генов, экспрессией которых они управляли. Последовательности многих из этих участков мало изменялись в процессе эволюции, в то время как другие участки, считавшиеся важными для управления клеткой, мутировали и изменялись в процессе эволюции с неожиданно высокой скоростью [10]. Все эти находки поставили большое количество новых вопросов, ответы на которые можно получить лишь в дальнейших исследованиях.
Другая задача, решение которой станет делом недалекого будущего, — определение последовательности оставшихся «малых» процентов генома, составляющих гетерохроматин, т. е. бедных генами и богатых повторами участков ДНК, необходимых для удвоения хромосом в процессе деления клетки. Наличие повторов делает задачу расшифровки этих последовательностей неразрешимой для существующих подходов, и, следовательно, требует изобретения новых методов. Поэтому не удивляйтесь, когда году в 2010 выйдет очередная статья, объявляющая об «окончании» расшифровки генома человека — в ней будет рассказано о том, как был «взломан» гетерохроматин.
Конечно, сейчас в нашем распоряжении имеется лишь некий «усредненный» вариант человеческого генома. Образно говоря — мы сегодня имеем лишь самое общее описание конструкции автомобиля: мотор, ходовая часть, колёса, руль, сиденья, краска, обивка, бензин с маслом и т. д. Ближайшее рассмотрение полученного результата свидетельствует о том, что впереди — годы работ по уточнению наших знаний по каждому конкретному геному. Программа «Геном человека» не прекратила свое существование, она лишь меняет ориентацию: от структурной геномики осуществляется переход к геномике функциональной, предназначенной установить, как управляются и работают гены. Более того, все люди на уровне генов отличаются так же, как одни и те же модели автомобилей отличаются различными вариантами исполнения одних и тех же агрегатов. Не только отдельные основания в последовательностях генов двух разных людей могут отличаться, но и количество копий крупных фрагментов ДНК, порой включающих в себя несколько генов, может сильно варьировать. А это означает, что на передний план выходят работы по детальному сравнению геномов, скажем, представителей различных человеческих популяций, этнических групп, и даже здоровых и больных людей. Современные технологии позволяют быстро и точно проводить такие сравнительные анализы, а ведь еще лет десять назад об этом никто и не мечтал. Изучением структурных вариаций человеческого генома занимается очередное международное научное объединение. В США и Европе значительные средства выделяются на финансирование биоинформатики — молодой науки, возникшей на стыке информатики, математики и биологии, без которой никак не разобраться в безграничном океане информации, накопленном в современной биологии. Биоинформационные методы помогут нам ответить на многие интереснейшие вопросы — «как происходила эволюция человека?», «какие гены определяют те или иные особенности человеческого организма?», «какие гены ответственны за предрасположенность к болезням?» Знаете, как говорят англичане: “This is the end of the beginning” — «Это конец начала». Вот именно эта фраза точно отражает нынешнюю ситуацию [12]. Начинается самое главное и — я совершенно уверен — самое интересное: накопление результатов, их сравнение и дальнейший анализ.
«…Сегодня мы выпускаем в свет первое издание „Книги жизни“ с нашими инструкциями, — сказал в эфире телеканала «Россия» Фрэнсис Коллинз. — Мы будем обращаться к нему десятки, сотни лет. И уже скоро люди зададутся вопросом, как они могли обходиться без этой информации».
Другую точку зрения можно проиллюстрировать, процитировав академика Кордюма В. А.:
«…Надежды же на то, что новая информация о функциях генома будет полностью открытой, чисто символические. Можно прогнозировать, что возникнут (на базе уже имеющихся) гигантские центры, которые смогут все данные соединить в одно связное целое, некую электронную версию Человека и реализовывать её практически — в гены, белки, клетки, ткани, органы и что угодно ещё. Но во что? Угодное кому? Для чего? В процессе работ по программе „геном человека“ стремительно совершенствовались методы и аппаратура для определения первичной последовательности ДНК. В крупнейших центрах это превратилось в некое подобие заводской деятельности. Но даже на уровне лабораторных индивидуальных приборов (вернее их комплексов) уже создано столь совершенное оборудование, что оно способно определить за три месяца такую по объему последовательность ДНК, которая равна всему геному человека. Не удивительно, что возникла (и тут же начала стремительно реализоваться) идея определения геномов индивидуальных людей. Безусловно, это очень интересно — сравнить отличия разных индивидуумов на уровне их первоосновы. Польза от такого сравнения тоже несомненная. Можно будет установить, у кого имеются какие нарушения в геноме, прогнозировать их последствия и устранить то, что может привести к болезням. Здоровье будет гарантированным, да и жизнь продлится весьма существенно. Это с одной стороны. С другой же стороны всё совсем не очевидно. Получить и проанализировать всю наследственность индивидуума означает получение полного, исчерпывающего биологического досье на него. Оно, при желании того, кто его знает, позволит столь же исчерпывающе делать с человеком всё что угодно. По уже известной цепочке: клетка — молекулярная машина; человек состоит из клеток; клетка во всех своих проявлениях и во всём диапазоне возможных ответов, записана в геноме; с геномом можно ограниченно уже и сегодня манипулировать, а в обозримом будущем вообще манипулировать практически как угодно…»
Однако, наверное, пугаться таких мрачных прогнозов еще рано (хотя знать о них, безусловно, нужно). Для их осуществления надо полностью перестраивать многие социальные и культурные традиции. Очень хорошо по этому поводу сказал в интервью доктор биологических наук Михаил Гельфанд, и. о. заместителя директора Института проблем передачи информации РАН: «…если у вас есть, предположим, один из пяти генов, предопределяющих развитие шизофрении, то что может случиться, если эта информация — ваш геном — попала в руки вашего потенциального работодателя, который ничего в геномике не понимает! (и как следствие — вас на работу могут не принять, посчитав это рискованным; и это не смотря на то, что шизофрении у вас нет и не будет — прим. автора.) Другой аспект: с появлением индивидуализированной медицины, основанной на геномике, полностью изменится страховая медицина. Ведь одно дело — предусматривать риски неизвестные, а другое дело — совершенно определенные. Если честно, то все западное общество в целом, не только российское, к геномной революции сейчас не готово…» [13].
Действительно, чтобы разумно пользоваться новой информацией, надо ее понимать. А для того чтобы понять геном — не просто прочитать, этого далеко не достаточно, — нам потребуются десятилетия. Слишком уж сложная картина вырисовывается, и чтобы осознать её, нам надо будет поменять многие стереотипы. Поэтому на самом деле расшифровка генома ещё продолжается и будет продолжаться. И будем ли мы стоять в стороне или станем, наконец, активными участниками этой гонки — зависит от нас.
- Киселёв Л. (2001). Новая биология началась в феврале 2001 года. «Наука и Жизнь»;
- Киселёв Л. (2002). Вторая жизнь генома: от структуры к функции. «Знание–Сила». 7;
- Смыслы «жизни»;
- Eric S. Lander, Lauren M. Linton, Bruce Birren, Chad Nusbaum, Michael C. Zody, et. al.. (2001). Initial sequencing and analysis of the human genome. Nature. 409, 860-921;
- J. Craig Venter, Mark D. Adams, Eugene W. Myers, Peter W. Li, Richard J. Mural, et. al.. (2001). The Sequence of the Human Genome. Science. 291, 1304-1351;
- Геном Нобелевского лауреата Джеймса Уотсона скоро будет расшифрован;
- International Human Genome Sequencing Consortium. (2004). Finishing the euchromatic sequence of the human genome. Nature. 431, 931-945;
- Геном человека: полезная книга, или глянцевый журнал?;
- Xinwei She, Zhaoshi Jiang, Royden A. Clark, Ge Liu, Ze Cheng, et. al.. (2004). Shotgun sequence assembly and recent segmental duplications within the human genome. Nature. 431, 927-930;
- «Мусорная» ДНК управляет эволюцией млекопитающих?;
- Ewan Birney, The ENCODE Project Consortium, John A. Stamatoyannopoulos, Anindya Dutta, Roderic Guigó, et. al.. (2007). Identification and analysis of functional elements in 1% of the human genome by the ENCODE pilot project. Nature. 447, 799-816;
- Lincoln D. Stein. (2004). Human genome: End of the beginning. Nature. 431, 915-916;
- Гельфанд М. (2007). Постгеномная эра. «Коммерческая биотехнология».
biomolecula.ru
